Покраснела кожа на яичках
Лабрадор 5 лет. 5 дней красные яички. назначили сначала цетрин, а потом дексаметазона 1 мл + Преднизолон мазь. Покраснения переходят в белые пятна и гноятся. Помогите советом. Других вариантов у меня нет. Перед этим был возможен контакт с крапивой и съел на улице по неосторожности куриное яйцо. До этого яйца ему не давали ни когда
Хронические болезни: Нет
На сервисе СпросиВрача доступна консультация ветеринара онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
Стероиды надо отменить если они не помогают.
Это может быть как местная реакция кожи, ( контактная, солнечный ожог, аллергическая, лишай, демодекоз, )так и более сложные ситуации(бактериальное, инфекции- бруцеллез, рикетсиоз, опухоли).
Надо сдать соскоб, посев на лишай. Цитологию с кожи возможно.
Надо сделать узи брюшной полости и семенников.
Сдать анализы крови, общий, биохимию.
Сдать анализ мочи общий
Сейчас надо одеть воротник.
Обработать Бравекто, симпарика, если не обработан.
Местно хлоргекседин, и мазь тридерм, 3 раза в день, до заживления.
Мягкая подстилка, ничем не перематывать.
Антибиотики системно хочется, но я бы пока воздержалась бы до анализов, так как разная причина требует разных антибиотиков.
Не хотелось бы прыгать с одного на другой.
Здравствуйте, видимо все-таки есть зуд и поэтому собака более активно чем обычно вылизывает эту область.
Для снятия зуда и воспаления наружно :
1) Хлорексидерм пенка с 4% хлоргексидином 7 мин подержать, затем смыть от 14 дней + Кортаванс спрей 2 раза в день от 14 дней / или Адвантан мазь тонким слое 2 раза в день 10 дней.
2) Для исключения самораразлизывания защитный воротник на 10 дней
Если не будет положительной динамики, нужно показать питомца врачу дерматологу и выяснить причину повышенного груминга.
Лептоспироз животных
Описание
Лептоспироз (другие названия желтуха, штутгартская болезнь, болезнь Вайля-Васильева) – тяжелое инфекционное заболевание, которому подвержены многие виды млекопитающих, в том числе собаки, а также человек.
Причиной лептоспироза является воздействие на организм возбудителя, которым являются бактерии рода Leptospira. Эти бактерии хорошо себя чувствуют и могут размножаться в стоячей теплой воде или в увлажненной почве, куда попадают в основном из мочи и выделений больных животных. Солнечные лучи или сильный нагрев убивают их, также губительно действуют разнообразные дезинфицирующие растворы.
В России болезнь у животных вызывают лептоспиры шести серологических групп, которые разделены на три самостоятельные группы: L. Icterohaemorrhagiae, L. canicolau, L. grippotyphosa. У собак чаще выделяют L. icterohaemorrhagiae и L.canicolau.
Желтуха у собак
К группе риска по лептоспирозу относят городских собак, особенно в раннем возрасте, а также охотничьих собак. Увеличение количества случаев заболевания происходит обычно в летний период, хотя заражение лептоспирозом не исключено и в холодное время года.
Чаще болеют лептоспирозом кобели, так как они проявляют наибольший интерес (обнюхивание, облизывание) к собачьим меткам. Основной путь проникновения возбудителя в организм – слизистые оболочки, возможна передача через открытые раны напрямую в кровь. Собака, искупавшаяся в стоячем водоеме, вполне может заболеть лептоспирозом. Также возможна передача возбудителя при бытовых контактах, через общий ошейник, во время «знакомства» собак на улице, через укусы клещей. Собаки могут заражаться лептоспирозом также при поедании крыс, мышей, сырого мяса, от больных домашних животных.
Исход болезни у непривитых собак в большинстве случаев летальный (до 90%). К сожалению, привитые собаки тоже имеют риск заразиться при неблагоприятной эпидемиологической обстановке. Переболевшие собаки остаются лептоспироносителями в течение трех лет и являются источником возбудителя болезни для животных и человека.
Стандартные схемы вакцинации (один раз в год) при неблагоприятной обстановке малоэффективны. В таких случаях рекомендуется вакцинация два раза в год. Больные лептоспирозом животные потенциально опасны для человека.
Развитие болезни лептоспироза
Проникнув в организм, лептоспиры активно передвигаются, размножаются, выделяют токсины. В ответ на это повышается температура, вырабатываются антитела, которые вызывают разрушение микробных тел. Это сопровождается освобождением эндотоксинов, которые, в свою очередь, вызывают гемолиз эритроцитов и высвобождение гемоглобина. Гемоглобин в больших количествах выделяется с мочой, окрашивая ее в красный цвет (гемоглобинурия). Кроме того, гемоглобин окрашивает кожу, слизистые оболочки и склеру в желто-красный цвет. Активизируются свертывающие системы крови. Кровеносные капилляры закупориваются кровяными сгустками, что приводит к некротизации обширных участков тканей и органов. Истощение свертывающих систем ведет к кровотечениям и кровоизлияниям. Микробные токсины и продукты распада клеток вызывают повреждение и воспаление печени, кишечника и других органов. Проникнув в почки, лептоспиры оказываются малодоступными для иммуноглобулинов и макрофагов. Может развиться острая почечная недостаточность.
Клинические признаки лептоспироза
Болезнь протекает остро и хронически. Острый лептоспироз протекает в двух клинических формах: геморрагической и желтушной. Инкубационный период при лептоспирозе собак составляет от 2 до 15 дней.
Для геморрагической формы типично резкое повышение температуры до 40,5-41,1’С, потеря аппетита, сухой потрескавшийся нос, зловонный запах изо рта. Слизистая рта ярко-красного, бордового цвета, позже на слизистых оболочках ротовой полости появляются кровоточащие язвочки. Этому сопутствуют рвота и понос с кровью. Иногда отмечалось самопроизвольное истечение крови и сукровицы из носа, анального отверстия. Животное быстро худеет, глаза западают, лимфоузлы увеличены.
В поздних стадиях заболевания отмечается мышечная дрожь, рвота с кровью, кровотечение из носа. Животное резко худеет, температура тела снижается ниже нормы (до 36-36,5 градусов). Моча выделяется в небольшом количестве, содержит желчь и белок.
Симптомы
Желтушная форма чаще регистрируется у щенков, но может развиваться и у взрослых животных. Болезнь может развиваться постепенно или оставаться незамеченной до появления выраженной желтухи. В начале заболевания по клиническим признакам часто напоминает парвовирусный энтерит: рвота, понос или запоры, шерсть тусклая, нередко с перхотью, студенистые выделения из глаз, от собаки исходит резкий неприятный запах. Печень, лимфоузлы увеличены.
Смертность собак при данной форме заболевания достигает 40-60%. Хронический лептоспироз часто протекает бессимптомно.
Диагностика лептоспироза
Для постановки диагноза проводят микроскопические исследования в тёмном поле микроскопа лептоспиры имеют вид тонких серебристых нитей, загнутых на одном или обоих концах, подвижны.
В крови животных обнаруживают не лептоспир, а антитела на это заболевание. Антитела вырабатываются иммунной системой животного в ответ на проникновение патогенного микроорганизма, в данном случае, на проникновение в организм лептоспир. Поэтому, чтобы диагноз был окончательным, необходимо через неделю повторить исследование. При лептоспирозе будет наблюдаться повышение титра антител в несколько раз.
Дифференциальный диагноз
Лептоспироз можно отличить от чумы наличием кровавой рвоты, повышенного количества белка в моче, наличие в ней желчных пигментов. Часто на ранней стадии заболевания дифференциировать чуму от лептоспироза можно только с помощью лабораторных исследований.
Лечение лептоспироза
Важно помнить, что любое лечение должно проводиться под наблюдением ветеринарного специалиста. Особенно это касается заболеваний с тяжелой формой течения. При любом серьезном заболевании очень важно своевременно начатое соответствующее лечение. В большинстве случаев самостоятельные попытки терапевтической помощи, оказанной в домашних условиях, приводят к плачевному результату. Когда такие животные попадают в ветеринарную клинику, к сожалению, вылечить их уже не удается. Заболевание прогрессирует достаточно быстро, разрушая и другие жизненно важные органы, поэтому каждый упущенный день, увы, оказывается не на пользу вашему любимцу.
Наилучший терапевтический эффект при лептоспирозе достигается сочетанием средств специфической и симптоматической терапии.
Специфическая терапия
В период циркуляции лептоспир в крови применяют антибиотик пенициллинового ряда, дигидрострептомицин и стрептомицин.
Симптоматическая терапия
Иммунитет
У выздоровевших собак образуется стойкий и напряженный иммунитет, который держится годами.
Как бороться с последствиями пищевого отравления
Пищевое отравление (интоксикация) — тяжелое функциональное расстройство со стороны желудочно-кишечного тракта, которое провоцируют болезнетворные микроорганизмы и продукты их жизнедеятельности (токсины), а также факторы, не имеющие отношение к патогенной микрофлоре. Среди населения чаще встречаются пищевые отравления, вызванные употреблением некачественной и термически необработанной пищи животного и растительного происхождения. Опасен не только любой из видов отравления в разгар болезни, но и последствия, с которыми сталкивается человек уже после выздоровления.
Симптомы пищевого отравления
Сами болезнетворные микроорганизмы, продукты их жизнедейятельности или другие токсические вещества, агрессивно воздействуют на желудочно-кишечный тракт на всей его протяженности. Пищевое отравление сопровождается дегидратацией (обезвоживанием), повреждением слизистой оболочки желудка и кишечника, нарушением баланса кишечной микрофлоры.
Выделяют такие распространенные симптомы пищевого отравления:
Токсины, выделяемые патогенными микроорганизмами, негативно влияют на центр терморегуляции, находящийся в гипоталамусе. Результатом такого влияния становится озноб и лихорадочное состояние. Понос при пищевом отравлении имеет профузный характер. Диарея и рвота приводят к значительной потере жидкости организмом и развитию обезвоживания. Дегидратация или обезвоживание сопровождается учащением пульса и повышением артериального давления.
Первые симптомы интоксикации дают о себе знать в течение 24 часов с момента попадания в организм болезнетворных микроорганизмов и других токсических соединений. В зависимости от тяжести отравления, температура тела может находиться в пределах от 37,3-40 градусов.
Классификация пищевых отравлений
Пищевые токсикоинфекции подразделяются на 2 основные группы:
Также, пищевое отравление может развиваться при попадании в организм солей тяжелых металлов, пестицидов, нитрозаминов и циклических углеводородов.
Первая помощь при пищевом отравлении
При возникновении симптомов пищевой токсикоинфекции, необходимо действовать по такому алгоритму:
Питание после отравления
Для того чтобы не ухудшить общее состояние, важно знать, что можно есть после отравления, а от чего лучше отказаться. Начинать прием пищи, рекомендовано на вторые сутки после отравления. Начинать следует с не крепкого куриного бульона, переходя на протертые супы из риса. В рацион включают слабый черный чай без сахара, вчерашний белый хлеб, сухари и сушки, запеченные яблоки без сахара, манную, овсяную, гречневую каши на воде, нежирную рыбу, приготовленную на пару или в отварном виде.
Из рациона исключают полуфабрикаты, жареную и жирную пищу, жирные сорта мяса и рыбы, овощи и фрукты в свежем виде, кондитерские изделия, выпечку, соусы, приправы, специи, фастфуд. Употребляемая пища не должна создавать дополнительную нагрузку на пищеварительную систему, не должна провоцировать диарею и раздражение слизистой оболочки ЖКТ. После перенесенной пищевой токсикоинфекции очень важно позаботиться о восстановлении микрофлоры кишечника, так как в 75% случаев, после отравления развивается кишечный дисбиоз.
Для самостоятельного восстановления нормальной микрофлоры организму потребуется много времени, и он не сможет осуществить это в полной мере. Возникает вопрос о том, как восстановить микрофлору кишечника, прибегнув к помощи извне. Метапребиотики это настоящая скорая помощь для организма, ослабленного пищевым отравлением и его последствиями.
Стимбифид Плюс — принципиально новое средство, в состав которого входят фруктополисахариды и фруктоолигосахариды, а также лактат кальция. В совокупности эти компоненты активно восстанавливают баланс кишечной микрофлоры, обеспечиваюи ее натуральным питательным субстратом и препятствуют размножению болезнетворных микроорганизмов.
Клинически доказано, что даже лучший пребиотик из числа современных наименований, не конкурирует по уровню эффективности с метапребиотиками. Метапребиотик Стимбифид Плюс не только предупреждает и лечит дисбактериоз после пищевого отравления, но и помогает бережно восстановить эпителий желудочно-кишечного тракта, который был поврежден продуктами жизнедеятельности бактерий и другими токсическими компонентами.
Кроме того, при тяжелых пищевых отравления могут назначаться антибиотики. Стимбифид Плюс поможет избежать последствий антибиотикотерапии. Начинать прием метапребиотика необходимо как можно раньше, и продолжать пить Стимбифид Плюс в течение 1,5-2 недель после нормализации общего состояния.
Орхит у собак
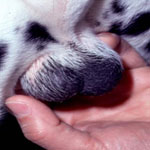
Орхит наиболее часто бывает у взрослых животных, старше 4-х лет.
Причины орхита. В зависимости от причины вызвавшей орхит, воспаление яичек у собак принято делить на:
Симптомы. Острый орхит проявляется у собаки общим угнетением, с редкими приступами беспокойства, повышается температура тела, происходит опухание и увеличение в размере мошонки. Кожа мошонки бывает покрасневшей или может иметь синюшный оттенок. При пальпации области мошонки ветеринарный специалист отмечает сильную болезненность одного или обоих яичек. Кобель осторожно и медленно передвигается, при ходьбе широко расставляет задние конечности.
В редких случаях без должного лечения воспаление яичек у собак принимает гнойный характер и может осложниться абсцессом и образованием свища в мошонке. При этом из мошонки выделяется густой сметанообразный гной, иногда с примесью крови.
Хроническое воспаление семенников у собак бывает редко, в основном при обострение воспалительного процесса или когда соединительная ткань начинает разрастаться в яичках и семенники начинают увеличиваться в размерах и чрезмерно отвердевают.
Диагноз. Диагноз на орхит ветеринарные специалисты клиники ставят на основании сбора анамнеза (травма области мошонки, драка с другой собакой и т.д.), клинического осмотра с пальпацией мошонки. Исследование крови в ветеринарной лаборатории на инфекционные заболевания (бруцеллез, лептоспироз и т.д.).
УЗИ брюшной полости позволит выявить цистит (цистит у собак), уретрит (уретрит у собак), простатит (простатит у собак) и другие патологии, приводящие к развитию эпидидимита у собак.
Дифференциальный диагноз. Орхит у собаки ветеринарные специалисты дифференцируют от новообразований (онкология у собак), инфекционных заболеваний (бруцеллез, лептоспироз).
Лечение. Лечение орхита у собак ветеринарными специалистами проводится в зависимости от причины вызвавшей воспаление яичек у собак.
Если причиной орхита у собак является инфекционное заболевание (бруцеллез, лептоспироз), то заболевших лептоспирозом собак изолируют и проводят комплексное лечение, включающее в себя этиотропную (специфическую) терапию –применение гипериммунной противолептоспирозной сыворотки и патогенетическую терапию. Гипериммунная противолептоспирозная сыворотка вводиться больным собакам подкожно в дозе 0,5мл на 1 кг массы тела один раз в сутки в течение 2-3дней. Сыворотка особенно эффективна, если ее применить в самом начале болезни. Проводится курс антибиотикотерапии препаратами группы пенициллина, которые эффективны в отношении лептоспир различных серогрупп (бензилпенициллин, бициллин-1, бициллин-3). Доза бициллиновых препаратов: 10-20тыс. ЕД на 1кг массы животного 1 раз в 3дня (2раза в неделю). Для прекращения лептоспиремии курс лечения антибиотиками должен состоять из 2 – 6 инъекций. Эффективным считается применение стрептомицина в дозе 10-15 тыс ЕД на 1 кг массы тела собаки 2 раза в сутки в течение 5 дней.
Если патогенные микроорганизмы в семенники собак попали из других мочеполовых органов, то проводится курс антибиотикотерапии, антибиотиками широкого спектра действия. Сегодня ветеринарные специалисты чаще всего применяют фторхинолы (пефлоксацин и офлоксацин), а также ветеринарный препарат – офлоксацинвет 10% в дозе 5мл на 10кг живого веса собаки, препарат вводят один раз в сутки. Из антибиотиков также рекомендуется принимать цефалоспорины (цефепи, цефуроксим и др.). Курс лечения цефалосплоринами составляет 7-10 дней.
При травматических орхитах, назначают обезболивающие препараты (амидопирин, анальгин) и проводят поясничную новокаиновую блокаду.
Если опухание яичек сопровождает высокой температурой тела, назначают курс антибиотиков.
При абсцессах мошонки, ее вскрывают, промывают антибактериальными растворами, если необходимо делается дренаж для оттока воспалительного экссудата. Назначается курс антибиотикотерапии.
Для предупреждения развития осложнений больной собаке назначают гепатопротекторы, пробиотики.
В том случае, когда владельцы собаки за ветеринарной помощью долго не обращались и воспаление семенников зашло далеко, проводят кастрацию кобеля. Кастрацию кобеля также проводят старым собакам и тем, которые не предоставляют племенной ценности.
Профилактика. С целью профилактики заболевания собак орхитом владельцы собак должны их вакцинировать против инфекционных заболеваний распространенных в регионе проживания, в том числе против лептоспироза (подготовка домашних животных к вакцинации и виды вакцин).
Во избежание получения травм в области мошонки во время драк с другими собаками необходимо кобеля выгуливать на поводке. При получении травм в области мошонки своевременно обращаться за ветеринарной помощью в ветеринарную клинику.
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
















