Как проявляется лямблиоз у взрослых
Среди всех протозойных заболеваний, лямблиоз у взрослых занимает лидирующие позиции. Заболеваемости лямблиозом в одинаковой степени подвержены все люди, независимо от пола и возраста. Эта патология вызывает тяжелые расстройства пищеварения, влияет на функциональное состояние органов желудочно-кишечного тракта и может провоцировать тяжёлые осложнения.
Характеристики лямблиоза
Лямблиоз относится к группе кишечных инфекций, и развивается при попадании лямблий в просвет тонкой кишки. Это заболевание распространено повсеместно, а в развитых странах заболеваемость лямблиозом составляет от 3 до 5%.В развивающихся странах, распространенность лямблиоза составляет от 10 до 15%. Повышенному риску заболеваемости этой протозойной инфекцией подвержены дети, посещающие дошкольные и школьные учреждения.
Причины развития
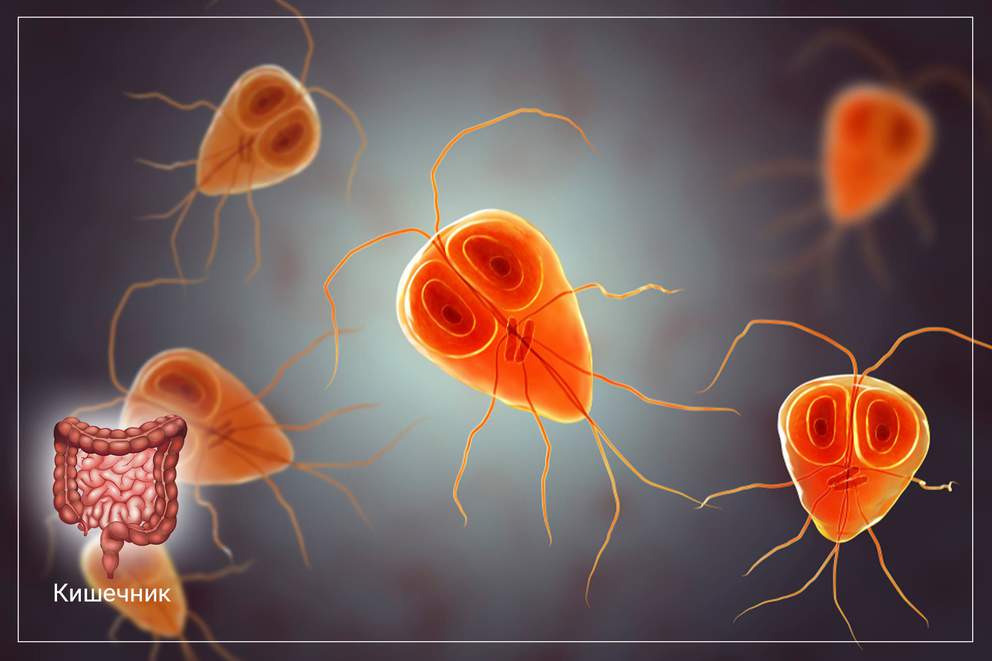
По своей природе, лямблии являются простейшими одноклеточными паразитами. Питаются эти микроорганизмы с помощью осмоса. Источником распространения инфекции является больной человек, который выделяет лямблий с испражнениями в окружающую среду. Распространителями лямблиоза, также могут быть животные (морские свинки, кошки, кролики, собаки). Благоприятные условия для распространения инфекции и инфицирования людей создаются районах с низким качеством питьевой воды, при недостаточном уровне навыков личной гигиены среди населения, а также при большой скученности людей.
К предрасполагающим факторам развития лямблиоза, можно отнести:
Клинические симптомы
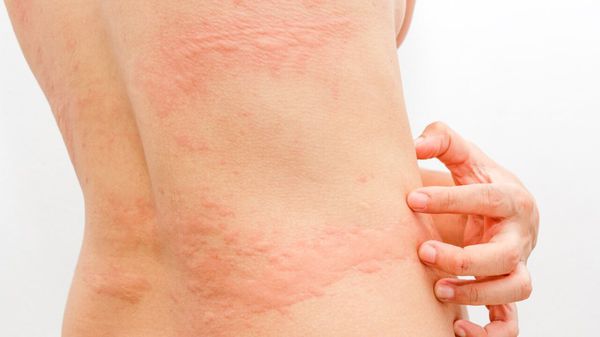
С момента проникновения возбудителей лямблиоза во внутреннюю среду организма и до момента появления клинических симптомов проходит от 1 до 3-х недель. К основным симптомам лямблиоза у взрослых можно отнести:
Острая фаза клинических симптомов поражения тонкой кишки может продолжаться от 5 до 7 дней. После завершения острой фазы, лямблиоз самопроизвольно проходит или переходит в хроническое подострое течение.
От масштабов инвазивного поражения кишечника лямблиями напрямую зависит выраженность интоксикации. Кроме перечисленных симптомов, лямблиоз может сопровождаться увеличением температуры тела до субфебрильных показателей, увеличением регионарных лимфатических узлов, быстрой утомляемостью, бруксизмом и эмоциональной лабильностью. Если данное заболевание развивается в детском возрасте, то оно нередко сопровождается гиперкинезами, снижением артериального давления и обморочными состояниями.
Методы диагностики
Клинические симптомы лямблиоза неспецифичны, поэтому диагностировать данную патологию на основании жалоб невозможно. Для диагностики лямблиоза назначаются такие методы обследования:
Лечение
Комплексное лечение лямблиоза включает ряд таких последовательных этапов:
На завершающем этапе комплексного лечения важно позаботиться о восстановлении кишечной микрофлоры. С этой целью используются метапребиотики, которые стимулируют рост и размножение естественной кишечной микрофлоры. Метапребиотик Стимбифид плюс восстанавливает популяцию собственных бифидумбактерий человека, количество которых значительно уменьшается при лямблиозе. Данное средство используется для лечения кишечных инфекций и их профилактики.
Кроме того, Стимбифид Плюс стимулирует иммунитет и ускоряет процесс регенерации кишечного эпителия. Метапребиотик может быть использован для профилактики лямблиоза у детей с 3-х лет. Средство благоприятно воспринимается организмом взрослых и детей, а также помогает ускорить процесс выздоровления при лямблиозе.
Акции
Лабораторное исследование кала включает в себя макроскопический, биохимический и микроскопический методы исследования. Доставлять материал для анализа следует в максимально короткие сроки.
Макроскопическое исследование
Простой осмотр каловых масс позволяет обнаружить взрослых гельминтов, членики ленточных гельминтов, определить характер кормления животного, наличие нежелательных компонентов (острые кости, палки, веревки, полиэтилен и т.д.). Основными показателями макроскопического исследования являются:
Цвет в норме коричневый, становится желтым при молочной диете, темно-коричневым при мясной. Черный цвет фекалии приобретают при кровотечении в переднем отделе ЖКТ (желудок, двенадцатиперстной и тонкой кишке).
Темно-коричневый наблюдается при недостаточности желудочного пищеварения, гнилостной диспепсии, колите с запором, колите с изъязвлениями, повышенной секреторной функции толстой кишки. Светло-коричневым становится ускоренной эвакуации из толстой кишки. Красноватый цвет обусловлен наличием кровотечения в задних отделах ЖКТ. Желтый цвет наблюдается при недостаточности переваривания в тонкой кишке и бродильной диспепсии. Серый цвет обусловлен недостаточностью поджелудочной железы. Белым становится при интрагепатальном застое или полной обтурации общего желчного протока.
Микроскопическое исследование
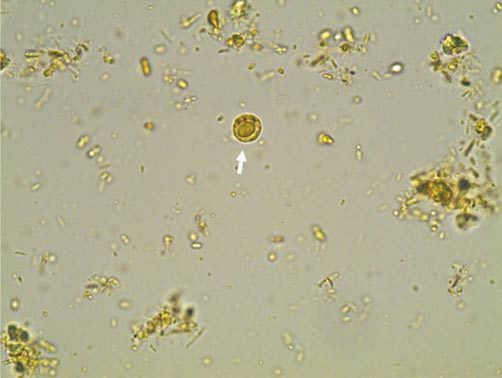
При микроскопии могут обнаруживаться яйца гельминтов, простейшие или их цисты, мышечные волокна (при недостаточности переваривания в желудке), жировые компоненты корма (при поражении поджелудочной железы, нарушении желчеотделения, нарушении всасывания в тонкой кишке), крахмал, клетчатка, лейкоциты, эритроциты, клетки эпителия, опухолевые клетки, кристаллы. Также можно обнаружить артефакты (попадают извне, например блохи, клещи и т.д.).
Биохимическое исследование
Биохимические показатели указываются в крестах, так как являются качественными, а не количественными.
Белок
Положительная реакция на белок указывает на наличие непереваренного или неусвоенного пищевого белка. Белок появляется при поражении желудка (гастрит, язва, новообразование), двенадцатиперстной кишки (дуоденит, язва, рак), тонкой, толстой и прямой кишок.
Кровь
Это реакция на скрытую кровь, не выявляемую макроскопически. Обнаруживает кровь при кровотечениях из всех отделов пищеварительного тракта (десен, пищевода, желудка и т.д.). Реакция может быть ложноположительной в присутствии пероксидаз бактерий, грибов, лекарственных препаратов, содержащих железо. Также она будет положительна при поедании животным сырого мяса.
Стеркобилиноген
Образуется из билирубина желчи. Как следствие его отсутствие в кале говорит об обтурации желчевыводящих путей. При скрытом дисбактериозе содержание стеркобилиногена снижено и обнаруживается билирубин.
Билирубин
Его обнаружение в кале указывает на следующие патологии: быстрая эвакуация кала по кишечнику, тяжелый дисбактериоз (отсутствие в толстой кишке нормальной микрофлоры).
Литература:
И.И. Миронова, Л.А. Романов, В.В. Долгов «Общеклинические исследования: моча, кал, ликвор, мокрота»; Москва 2009
А. Хэм, Д. Кормак «Гистология» том 4; Москва «Мир» 1983
С.Ю. Зайцев, Ю.В. Конопатов «Биохимия животных, фундаментальные и клинические аспекты» СПб, Москва, Краснодар 2004
Не спешите выбрасывать кошку!
Миф №1. Беременным нельзя держать кошек и собак, так как можно заразиться токсоплазмозом
На самом деле: НЕ СОВСЕМ ТАК
Основные «хозяева» токсоплазмы (Toxoplasma gondii), которая относится к простейшим — кошки, в том числе домашние и бродячие. Ооцисты (особая форма возбудителя) токсоплазмы, способные нанести вред здоровью, находятся в фекалиях кошек и на шерсти. Проникая в организм человека, они поражают различные органы и ткани (печень, селезенка, нервная система, глаза, миокард сердца, легочный эпителий, скелетные мышцы).
Заразиться токсоплазмозом при контакте с загрязненными кошачьими испражнениями действительно можно. Но для чтобы стать опасной для человека, токсоплазма должна из ооцисты превратиться в личинку — период занимает 4-5 дней. А это значит, что ежедневная уборка кошачьего лотка, ветеринарный контроль животного и регулярная антигельминтная обработка — убережет от паразита. А вот бездомных животных гладить все-таки не рекомендуется.
Важно помнить, что токсоплазмоз также передается при употреблении недостаточно термически обработанного мяса, содержащего цисты (баранина, свинина). Поэтому беременным категорически не рекомендуется употреблять недостаточно прожаренную свинину, баранину («мясо с кровью»).
Миф №2. Симптомы токсоплазмоза схожи с симптомами гриппа
На самом деле: ДА
Инфицирование токсоплазмозом может протекать бессимптомно, но довольно часто на ранних стадиях вызывает симптомы схожие с гриппом (озноб, резкое повышение температуры и др.). Острый период может закончиться за несколько дней, а может растянуться до нескольких месяцев. Поэтому если вам кажется, что вы заболели и никак не вылечитесь, пройдите исследование на токсоплазмоз, чтобы исключить риск инфицирования.
Попадая в тело человека, ооцисты и тканевые цисты токсоплазм пронимают в клетки-макрофаги в кишечнике и уже через кровь «путешествую» по всему организму. Токсоплазма может зафиксироваться в печени или селезенке, ткани легких, мышечной ткани сердца с образованием скоплений. В организме эти скопления сохраняются до нескольких десятков лет, иногда пожизненно.
Хроническая стадия токсоплазмоза протекает скрыто и наиболее опасна для людей с ослабленным иммунитетом (беременные, ВИЧ, гепатит, хроническое воспаление и др.), так как может вызвать токсоплазменный энцефалит, приводящий к летальному исходу.
Миф №3. Обычные мухи переносят возбудителей амёбиоза
На самом деле: ДА
Заразиться амёбиозом можно через грязные руки, а также при непосредственном контакте с носителем цист (особая форма возбудителя). В распространении цист также участвуют обычные мухи, они являются механическими переносчиками.
Дизентерийная амеба (Entamoeba histolytica) распространена повсеместно. Это микроскопическое простейшее обитает и в воде, и в почве, «выживает» на кожице фруктов и овощей.
Состоящая всего из одной (!) клетки, амёба может нанести непоправимый урон здоровью. В ослабленном организме, при инфекции или переохлаждении, она переходит в опасную патогенную форму. Выделяя особый протеолитический фермент, и вызывая кишечные язвы и кровотечения, она тем самым добывает себе «еду» — эритроциты (красные кровяные клетки). Поэтому на фоне амёбиоза часто развиваются анемии, общая интоксикация.
Место обитания в теле человека — просвет толстого кишечника и его стенки. Однако с током крови амёбы могут разноситься по всему организму и локализоваться в легких, головном мозге и даже в коже.
Чаще всего амёбиоз встречается в странах с жарким и теплым климатом (ближний Восток, страны Юго-Восточной Азии). В этом случае рекомендуется соблюдать несложные правила защиты:
Миф №4 Лямблиоз поражает желчный пузырь
На самом деле: ДА
Как и цисты амёб, цисты лямблий могут длительно сохранять свою активность на плохо промытых овощах, фруктах, зелени, в воде (до 70 суток), и даже в пыли. Переносчиком лямблиоза также могут быть мухи: поэтому летом, на даче или на отдыхе, не оставляйте еду не прикрытой.
Основная мишень лямблий — желчный пузырь, двенадцатиперстная кишка и тонкий кишечник. Блокируя слизистую оболочку, простейшие буквально тормозят нормальный процесс пищеварения. Пища не переваривается, начинаются процессы гниения и размножения бактерий и дрожжевых грибков.
В результате чего нарастают симптомы интоксикации, нарушается всасывание питательных веществ — белков, жиров, углеводов, что может привести к истощению.
Миф №5 При паразитарной инфекции человек стремительно худеет
На самом деле: НЕ СОВСЕМ ТАК
При паразитарной инфекции симптомов может не быть вовсе или они будут не явными. К основным симптомам, которые должны насторожить относятся повторяющие эпизоды:
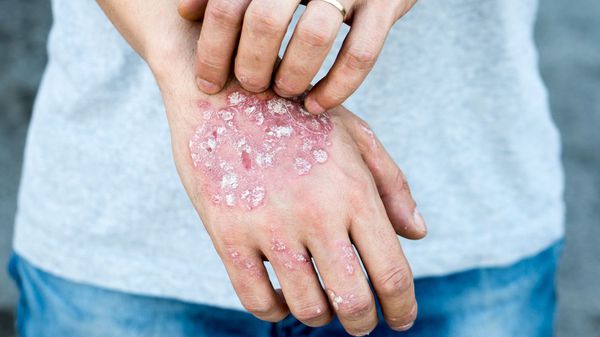
При заражении ленточными червями часто возникают аллергические реакции (высыпания, зуд кожи), повышение температуры тела, проблемы неврологического характера, такие как судороги.
При нематодной инфекции (аскариды, власоглав, трихостронгилида, кривоголовка двенадцатиперстная, томинкс, некатор) появляется кожная сыпь, зуд, усталость, состояние, характерное для анемии. При трихинеллезе нередко заметен отек лица, ощущаются мышечные боли, повышенная светочувствительность, может возникнуть конъюнктивит.
Миф №6. При употреблении суши, сашими и роллов со свежей рыбой можно заразиться паразитическими червями
На самом деле: ДА
Не хотим никого пугать, но в сырой, а также в недостаточно проваренной рыбе могут содержаться личинки широкого лентеца (вид ленточных паразитических червей). Попадая в тонкий кишечник, в течение 2-х месяцев они превращаются во взрослых особей. Живут в теле «хозяина» до 20 лет, достигая в размерах до 10 метров.
Черви истребляют полезную микрофлору кишечника, которая производит фолиевую кислоту, необходимую для кроветворения, «поедая» витамин B12. В результате чего развиваются тяжелые анемии.
Миф №7 Для диагностики паразитов можно сдать только кровь
На самом деле: НЕТ
Для диагностики паразитарной инфекции используют кровь (для выявления антител к возбудителю) и кал — для микроскопического исследования на яйца глист и простейшие. Его проводят обычным способом и методом обогащения (система ПАРАСЕП). Анализ кала методом обогащения (система ПАРАСЕП) более чувствителен, что позволяет выявить наиболее сложных в плане диагностики паразитов — например, описторхов (очень мелкие яйца) и простейших (амебы).
При подозрении на паразитарную инфекцию, а также для оценки контроля эффективности противопаразитарного лечения, в случае заражения, в СИТИЛАБ Вы можете выполнить все необходимые диагностические исследования:
Кровь сдается натощак или не ранее, чем через 8 часов после приема пищи. Перед взятием крови за полчаса не рекомендуется курить, не употреблять кофе. Можно пить негазированную воду.
За 72 часа до сдачи кала на исследование исключить прием слабительных, ректальных свечей, масел, медикаментов, оказывающих влияние на перистальтику кишечника (белладонна, пилокарпин и др.) и на окраску кала (железо, висмут, сернокислый барий).
Что такое бластоцистоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
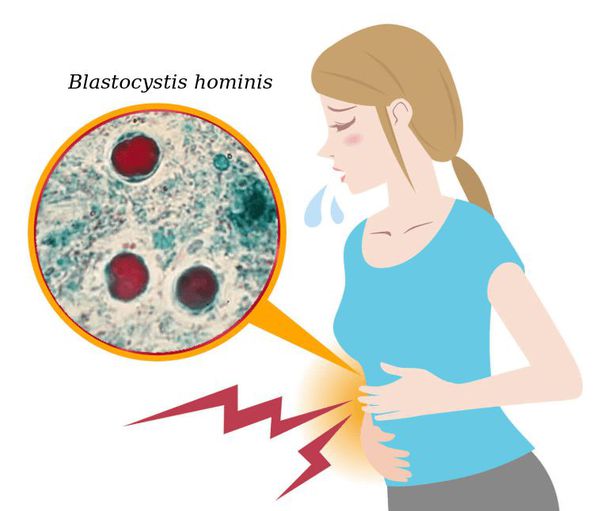
Бластоцистоз — это заболевание человека, вызываемое простейшим одноклеточным микроорганизмом Blastocystis, который колонизирует желудочно-кишечный тракт и при определённых условиях вызывает срыв функционирования кишечника (запоры или диарея, дискомфорт и боли в животе). Также Blastocystis повышает частоту развития иммунодепрессии, проблемной кожи и патологии суставов. Паразит проникает в организм посредством фекально-орального механизма. Чаще всего болезнь протекает в форме неактивного носительства.
Этиология
Впервые эти простейшие были описаны А. Алексеевым (А. Alexieff) в 1911 году, а уже в 1912 году Е. Брумпт (Е. Brumpt) выделил и описал основные признаки бластоцисты в материале человека.
Для людей характерно нахождение подтипа ST (при генетическом типировании). Всего 9 видов (ST1-ST9), наиболее распространены ST1, ST2, ST3 и ST4, причём они могут сосуществовать в организме одного хозяина в разных сочетаниях. На сегодняшний день конкретная патогенность разных подтипов для человека не выяснена, однако есть предположения, что заболевание вызывают лишь некоторые подтипы паразита, тогда как другие в основном приводят лишь к носительству.
Жизненный цикл Blastocystis до конца не изучен. Размножаются микроорганизмы бинарным делением. Тело покрыто специальной мембраной, с которой соприкасается цитоплазма и органеллы. Паразиты могут находиться в кишечнике от недели до нескольких лет.
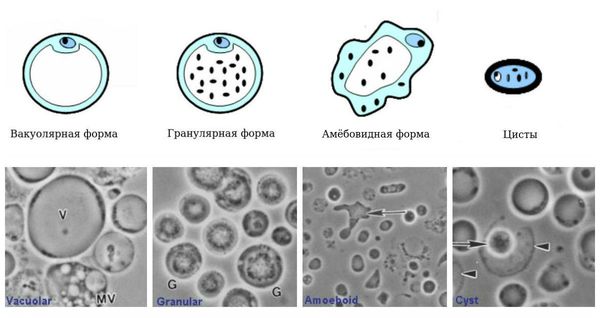
Бластоцисты имеют 4 формы жизни:
Паразиты к ультивируются на питательных средах, причём образуют множество нетипичных форм (промежуточные стадии развития).
Эпидемиология
Бластоцисты распространены повсеместно, это один из самых часто встречающихся паразитов в мире (заражены, вероятно, не менее 1 млрд. человек), распространённость подтипов пока изучается. В некоторых регионах, особенно в тропиках, ими инфицировано до 100 % населения, в США — около 23 % популяции. Заболеваемость выше в тех регионах, где присутствует антисанитария и не уделяется должного внимания соблюдению правил личной гигиены. Чаще болезнь выявляется среди людей, которые контактируют с животными и имеют сопутствующую патологию ЖКТ или хронический вирусный гепатит. Во многих случаях они выявляются в сочетании с другими патогенами ЖКТ (лямблиями, возбудителями острых кишечных инфекций и др.).
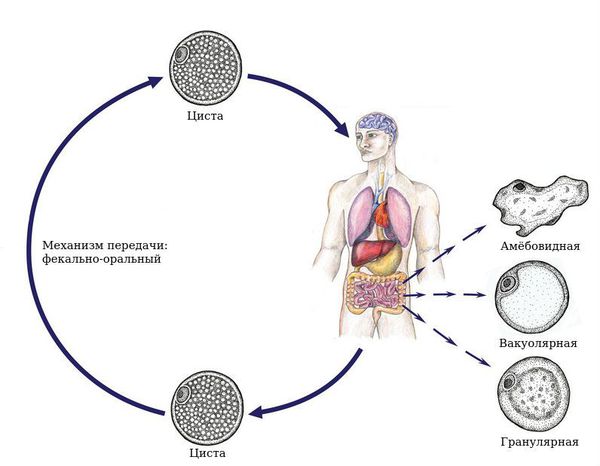
Механизм передачи — фекально-оральный, пути — водный (через загрязнённую воду), пищевой (через заражённую пищу) и контактно-бытовой (при несоблюдении правил гигиены, возможно распространение насекомыми, например мухами и тараканами).
Симптомы бластоцистоза
Во множестве случаев выявления бластоцист у людей симптомы не проявляются или их нельзя напрямую связать с паразитом (по крайней мере, на сегодняшнем уровне развития медицины). Возможно, люди (и врачи в том числе) оказались «ослеплены» фактами исчезновения и уменьшения количества некоторых паразитарных заболеваний (например, малярии и дракункулёза), что создало неверное представление о победе над паразитами. Однако постоянное увеличение числа больных с патологией кишечника неустановленной этиологии, иммунодефицитами и кожными заболеваниями может быть вызвано распространением именно тех микроорганизмов, которые раньше считались непатогенными или условно-патогенными.
Чаще всего при манифестной форме заболевания (когда болезнь начинает проявляться) больные указывают на следующие признаки:
Есть некоторые предпосылки, указывающие на более частое развитие манифестных форм болезни, в основном это:
Бластоцистоз у беременных
Патогенез бластоцистоза
Входные ворота для микроорганизма — ротовая полость. Далее бластоцисты проходят в неизменном виде через пищевод и желудок (не повреждаясь агрессивной средой желудка) и попадают в кишечник. Здесь происходит изменение цистной неактивной формы в более активную вегетативную (вероятно, в различные стадии жизненной формы в зависимости от условий и подтипа паразита) и дальнейшее нахождение паразита преимущественно в толстом кишечнике.
Бластоцисты могут нарушать расположение и функционирование актиновых филаментов эпителиальных клеток кишечника (нитей из специальных белков, находящихся в цитоплазме клеток, их основная функция — сократительная). Таким образом они влияют на барьерную функцию кишечной стенки, что приводит к диарее, нарушению процессов пищеварения и обмена биологически активных веществ.
Выявлена способность бластоцист стимулировать выработку провоспалительных цитокинов клетками толстого кишечника (ИЛ-8, гранулоцитарно-макрофагальный колониестимулирующий фактор), которые играют роль в развитии ревматоидного артрита.
Классификация и стадии развития бластоцистоза
Единой официально принятой классификации бластоцистоза не существует, обобщённо можно представить следующую градацию:
По клинической форме:
В Международной классификации болезней 10-го пересмотра (МКБ-10) о бластоцистозе нет информации. Однако заболевание можно отнести к группе А07 — Другие протозойные кишечные болезни.
Осложнения бластоцистоза
Диагностика бластоцистоза
Для верной диагностики важно целенаправленно определить бластоцисты в биологическом материале. Врач принимает решение, являются ли именно они причиной симптомов у конкретного человека: часто симптомы обнаруживаются в ассоциации с другими патогенами или имеется сопутствующая патология неинфекционного характера.
Дифференциальная диагностика
Лечение бластоцистоза
Терапия бессимптомного носительства в каком-либо медицинском вмешательстве не нуждается. Не стоит заниматься лечением и тем более самолечением при отсутствии симптоматики и сомнении в роли данного микроорганизма в болезни. Нет гарантии, что применение препаратов благотворно скажется на здоровье кишечной экологической системы и организма в целом и не ухудшит проявления заболевания.
При развитии симптомов, в патогенезе которых нельзя исключить роль бластоцист, и подтверждении паразитирования их в кишечнике проводятся следующие мероприятия:
Прогноз. Профилактика
При сохранном иммунитете прогноз благоприятный (даже при развитии клинически выраженного заболевания), при иммунодефиците (особенно СПИДе) прогноз серьёзный.
Меры профилактики неспецифичны, их можно разделить на общественно-значимые (социальные) и индивидуальные.
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).