Анализ на ПСА при простатите
Простспецифический антиген — результативный анализ для диагностирования рака предстательной железы. Однако показатели выше нормы не всегда говорят о заболевании раком. Для получения точного результата, необходимо правильно подготовится. Анализ ПСА при простатите необходимо регулярно сдавать для профилактического наблюдения. Для уверенности в мужском здоровье, даже при отсутствии симптоматики заболевания, врачи рекомендуют ежегодный мониторинг показателей антигена.
Что такое простатспецифический антиген, далее ПСА — вещество, выделяемое эпителием протоков предстательной железы, для разжижения семени и беспрепятственному движению сперматозоидов.
Показания к проведению исследования
При воспалительных процессах предстательная железа увеличивается, и уровень ПСА повышается. Также при повышенных показателях антигена врач может предположить развитие рака. Является онкомаркером.
Показания, для проведения анализа
Подготовка к сдаче
Для получения достоверных результатов должны быть соблюдены условия:
Следует помнить, что некоторые медицинские препараты могут повышать уровень антигена в крови, о приеме лекарств необходимо сообщить врачу.
До сдачи анализа необходимо воздержаться от:
Расшифровка результатов
При исследовании крови на ПСА выделяют два показателя:
Свободный показатель занимает 10% белка антигена и при подозрении на опухолевые процессы обращают внимание, особенно на этот вид.
Общий ПСА отвечает за дегенеративные изменения простаты. При повышении общего уровня антигена врач может предположить развитие простатита или аденомы простаты, диагноз ставится при соотношении свободного и связанного белка антигена и только при изучении полной истории болезни.
Однако для полной картины необходимо учитывать процентное соотношение друг к другу обоих показателей.
Нормы ПСА зависят от возраста исследуемого.
Не всегда большое значение ПСА означает рак, при простатите (не хроническом), аденоме простаты показатели могут быть завышены. При таких результатах врач-уролог назначает дополнительное исследование в виде биопсии тканей предстательной железы, ультразвуковое исследование, компьютерную томографию.
При остром течении простатита концентрация белка антигена может увеличиваться до 10 нг/мл, это не является нормой и анализировать высокий уровень ПСА может только высококвалифицированный уролог. При аденоме простаты, простатите ПСА всегда повышен либо на высокой границе нормы, но это слишком серьезная проблема, чтобы оставлять ее без внимания. Необходимо проконсультироваться с урологом и сдать анализ крови на уровень ПСА в динамике, дабы картина болезни была более полной.
Биохимический рецидив рака предстательной железы после радикального лечения
 | Всеволод Борисович Матвеев Д.м.н., проф., заведующий отделением урологии РОНЦ им. Н.Н. Блохина РАМН vsevolodmatveev@mail.ru |
 | Мария Игоревна Волкова Ст. науч. сотр. отделения урологии РОНЦ им. Н.Н. Блохина РАМН mivolkova@rambler.ru |
Широкое внедрение оценки простатического специфического антигена (ПСА) в клиническую практику привело к «миграции» стадии рака предстательной железы (РПЖ) в сторону локализованных форм заболевания и закономерному увеличению доли радикальных методов терапии данной группы больных. В течение 10 лет после радикальной простатэктомии (РПЭ), дистанционной и внутритканевой лучевой терапии (ЛТ) или аблации у 27–53% пациентов развивается рецидив опухоли, по поводу которого в 16–53% случаев проводится лечение 2-й линии.
В 1999 г. в исследовании C.R. Pound было показано, что ни у одного больного рецидивы не диагностируются без сопутствующего повышения ПСА. С тех пор изолированное повышение этого маркера без клиникодиагностических признаков опухоли стали расценивать как ПСА-рецидив или так называемый биохимический рецидив. Определения биохимического рецидива после разных методов радикального лечения существенно различаются.
Определяемый ПСА после РПЭ может свидетельствовать как о рецидиве, так и о резидуальной ткани простаты без опухоли, оставленной по краю разреза. С целью стандартизации определения ПСА-рецидива после РПЭ предлагались различные пограничные значения маркера. Согласно решению международного консенсуса биохимическим рецидивом после хирургического лечения считается повышение ПСА >= 0,2 нг/мл как минимум в 2 измерениях.
Абсолютного значения пограничного уровня ПСА при рецидиве после ЛТ не существует. До 2006 г. общепринятым являлось определение ПСА-рецидива после ЛТ ASTRO (1996): повышение ПСА в 3 последовательных измерениях, выполненных с интервалом >= 6 мес. Однако данное определение не валидизировалось в отношении риска метастазирования и смерти от РПЖ. В связи с этим в 2006 г. на основании анализа специфической выживаемости было разработано новое определение ПСА-рецидива после ЛТ: увеличение ПСА на 2 нг/мл по сравнению с минимальным достигнутым значением маркера (надиром).
Относительно биохимического рецидива после аблативного лечения РПЖ нет единого мнения. Разные исследователи предлагают применять пограничные значения ПСА от 0,5 нг/мл до 1 нг/мл, определение ASTRO, а также прирост ПСА относительно надира.
С целью выявления факторов риска отдаленных метастазов при ПСА-рецидиве проводились многочисленные исследования. У больных, подвергнутых РПЭ, важнейшими факторами неблагоприятного прогноза метастазов считаются кинетика ПСА (скорость роста ПСА > 0,75 нг/мл/год, время удвоения ПСА T2, N+, сумма Глисона > 6). Отсутствие перечисленных факторов свидетельствует о том, что наиболее вероятным источником маркера служит местный рецидив. У облученных пациентов метастазы, вероятнее всего, служат причиной ПСА-рецидива при повышении маркера сразу после лечения ( = 18 мес после лечения).
Возможными подходами к ведению больных с ПСА-рецидивом РПЖ представляются динамическое наблюдение, спасительное местное лечение с целью эрадикации всех опухолевых клеток и паллиативная гормонотерапия (ГТ).
Как уже было отмечено выше, в большинстве случаев клиническое прогрессирование ПСА-рецидива после РПЭ реализуется крайне медленно. Однако показатель Глисона > 7, возникновение ПСА-рецидива через 2 года после радикального лечения, и временем удвоения ПСА > 10 мес.
Тщательно отобранным пациентам с повышением ПСА после РПЭ, обусловленным местным рецидивом, возможно проведение спасительной лучевой терапии (СЛТ). Ее лечебное значение не доказано. После окончания облучения неопределяемый ПСА регистрируется у 60–90% больных, однако в течение последующих 5 лет повторный ПСА-рецидив диагностируют в 10–45% случаев. Важнейшим фактором прогноза выживаемости без повторного ПСА-рецидива по окончании СЛТ является уровень ПСА до облучения. В разных исследованиях пограничное значение прогностически значимой концентрации ПСА колеблется от 0,5 до 2,5 нг/мл. СЛТ в дозе > 64 Гр достоверно увеличивает выживаемость без ПСАрецидива. На основании этих данных СЛТ рекомендуется больным с повышением ПСА после РПЭ 64 Гр.
Крупных исследований, посвященных паллиативной ГТ при ПСА-рецидиве после радикальных методов лечения, не проводилось. Оптимальные время начала, режим и вид эндокринного лечения у данной категории больных не определены. В регистровом исследовании ранняя ГТ приводила к увеличению времени до метастазов в группе неблагоприятного прогноза (сумма Глисона > 7, время удвоения ПСА 7 и категория N+, что необходимо учитывать при отборе больных для проведения интермиттирующей андрогенной аблации.
Среди больных с биохимическим рецидивом РПЖ после ЛТ 5 лет переживает 76% мужчин. Важнейшими факторами неблагоприятного прогноза появления отдаленных метастазов считаются надир ПСА >= 1,5 нг/мл и сумма Глисона > 6. Проведение ГТ достоверно увеличивает 5-летнюю выживаемость без отдаленных метастазов, но данная закономерность сохраняется только в подгруппе пациентов с малым временем удвоения ПСА, т. е. высокой вероятностью того, что повышение ПСА обусловлено метастазированием опухоли. Среди больных со временем удвоения ПСА больше года андрогенная аблация не влияет на результаты лечения. На основании этих данных Pinover и соавт. разработали алгоритм выбора лечебной тактики при ПСА-рецидиве после ЛТ, принятый во многих клиниках мира. Пациентам со временем удвоения ПСА >= 12 мес, надиром ПСА 10 лет без метастазов и ПСА Средняя оценка:
Биохимический рецидив после радикальной простатэктомии: немедленная или отсроченная гормональная терапия
 | Всеволод Борисович Матвеев Д.м.н., проф., заведующий отделением урологии РОНЦ им. Н.Н. Блохина РАМН vsevolodmatveev@mail.ru |
 | Виталий Александрович Черняев Врач-онколог отделения урологии ГУ РОНЦ им. Н.Н. Блохина РАМН chercrc@gmail.com |
Как известно, заболеваемость злокачественными новообразованиями предстательной железы увеличивается как во всем мире, так и в России. При этом благодаря широкому внедрению в клиническую практику определения сывороточного содержания простатического специфического антигена (ПСА) все в большем проценте случаев удается диагностировать заболевание на ранних стадиях, что делает возможным выполнение радикального хирургического лечения.
Однако особенности течения заболевания таковы, что у некоторых пациентов развивается рецидив заболевания отмечается постепенное увеличение показателей ПСА биохимический рецидив (БР). При этом по времени развития БР и скорости прироста ПСА можно предположить характер рецидива. Если БР наступает более чем через 2 года после радикального хирургического лечения и характеризуется временем удвоения ПСА (PSADT) > 12 месяцев, можно думать о местном рецидиве заболевания. В таком случае основным методом лечения является проведение дистанционной лучевой терапии. При быстром развитии БР (менее 2 лет после радикального лечения) и быстром PSADT (менее 12 месяцев), вероятно, речь идет о системном рецидиве. В таком случае показано проведение гормональной терапии. При этом до сих пор продолжается дискуссия о сроках назначения гормональной терапии (немедленная или при появлении клинических симптомов). На сегодняшний день, согласно рекомендациям Европейской ассоциации урологов, под БР после радикального хирургического лечения понимают увеличение ПСА более 0,2 нг/мл.
Частота развития БР составляет от 19 до 75%. Приведенные данные основываются на результатах ретроспективного исследования Karakiewicz et al. (Urology, 2005), объединившего опыт 8 клиник (5831 пациент). В исследовании было показано, что риск развития БР зависит от нескольких факторов: местной распространенности опухолевого процесса, степени дифференцировки (показатель Глисона), наличия метастатического поражения лимфатических узлов, присутствия положительного хирургического края.
На сегодняшний день не было проведено крупных рандомизированных исследований, напрямую сравнивающих результаты лечения при применении немедленной и отсроченной гормональной терапии при развитии БР после радикального хирургического лечения. Поэтому для выяснения преимуществ того или иного подхода приходится экстраполировать данные, полученные при сравнении немедленной или отсроченной гормональной андрогендепривационной терапии (АДТ) при лечении пациентов, которым не было проведено радикального хирургического лечения.
Ниже приведены результаты 2 наиболее значимых подобных исследований. Это протоколы EORTC 30846 (Schroder et al., 2004) и 30891 (Studer et al., 2006). Дизайн 2 упомянутых протоколов примерно схож. В исследования включались пациенты с первичным бессимптомным РПЖ сТ1-4Ш-Ш0, которым по тем или иным причинам не было проведено радикального хирургического лечения. Пациентов разделили на 2 группы: пациенты 1-й группы получали немедленную гормональную терапию (аналоги ЛГРГ или билатеральную орхидэктомию), для пациентов 2-й группы лечение начиналось только при клиническом проявлении метастазов или обструкции мочеточников (противопоказание растущий уровень ПСА). При анализе результатов лечения показатели общей выживаемости и опухолевоспецифической выживаемости достоверно не различались. Однако при более детальном рассмотрении оказалось, что в результате немедленной гормональной терапии достоверное преимущество в общей выживаемости имели пациенты, ПСА которых был более 20 нг/мл в возрастной группе 70 лет.
Влияет ли немедленная АДТ на развитие отдаленных метастазов? Данной проблеме было посвящено исследование Moul et al. (2004). Были изучены результаты лечения около 5000 пациентов, которым была выполнена РПЭ по поводу РПЖ. У 27,2% пациентов развился БР. Пациенты были разделены на 2 группы: немедленной и отсроченной АДТ. В общей когорте пациентов не было показано преимущества немедленной АДТ. Однако, в группе пациентов, у которых балл Глисона > 7 и PSADT 20 нг/мл), местно-распространенный РПЖ рТ3-4, подтверждено наличие метастатического поражения лимфатических узлов, быстро увеличивается показатель ПСА после радикального хирургического лечения (PSADT 3 лет после простатэктомии
О чем говорит повышение ПСА у мужчин
Простатспецифический антиген — это опухолевый маркер, который применяется для диагностики рака и аденомы простаты. Его определяют в сыворотке крови. Повышение ПСА — один из недобрых «звоночков», говорящих о проблемах с предстательной железой. Причины плохого анализа могут быть разными.
Важно! Тест показывает нарушение деятельности железы, а не обязательное наличие рака или аденомы. В исследованиях рак простаты был обнаружен у 30% мужчин с повышенным ПСА. В остальных случаях наблюдались другие заболевания: простатит, инфекции мочеполовой системы и т. д.
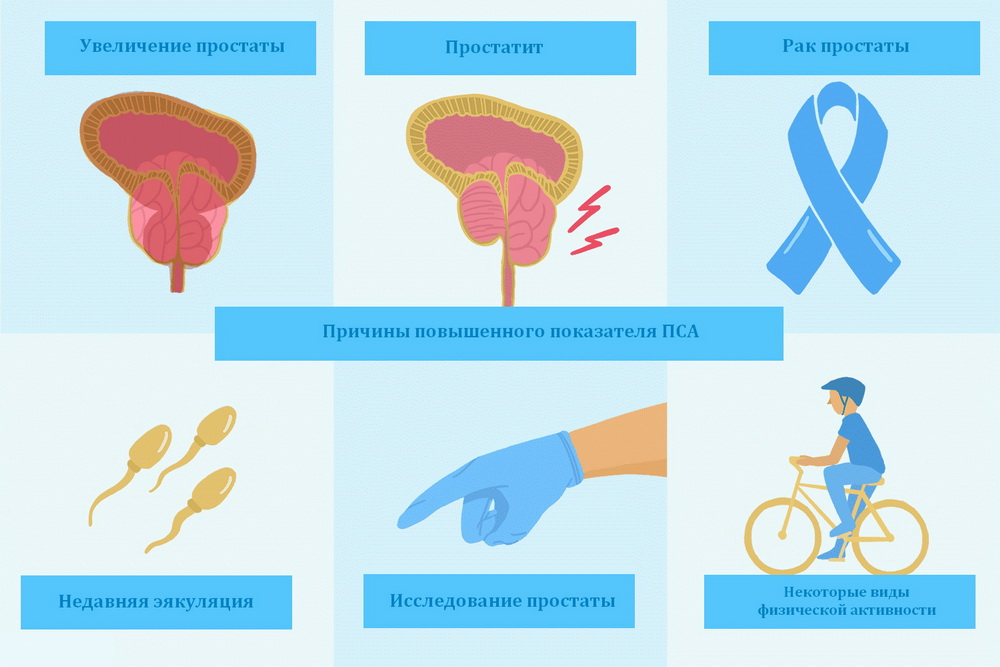
Причины изменения уровня простатспецифического антигена
В зависимости от болезни могут изменяться причины, почему повышается ПСА у мужчин:
Как видите, причины, почему повышается ПСА, у каждого заболевания свои. Наличие перечисленных симптомов позволяет сделать более точный вывод о наличии или отсутствии рака у мужчины.
Интересно, что врачи против регулярного скрининга на ПСА здоровых мужчин. Считается, что это может привести к «гипердиагностике» и «избыточному лечению». Многие заболевания и процессы, вызывающие повышение ПСА, протекают бессимптомно годами, а медицинское вмешательство вполне может вызвать осложнения.
Что может резко повысить ПСА?
Нередко неуверенные в словах уролога мужчины сдают анализ несколько раз. Что делать, если на одном из тестов резко повысился ПСА? Волноваться не стоит, скорее всего, это связано с неправильной подготовкой к анализу. Суточные колебания маркера в сыворотке крови не значительны, но есть другие факторы, оказывающие влияние на результат. В каких случаях повышается ПСА у мужчин:
Правильная подготовка и учет всех сопутствующих факторов, будь то операции или исследования органа, позволяют врачу понять, что означает повышение ПСА в данном конкретном случае, корректно интерпретировать результаты.
Волнуетесь за свое здоровье? Есть неприятные симптомы? Клиника урологии имени Р. М. Фронштейна Первого Московского Государственного Медицинского Университета имени И.М. Сеченова (Государственный центр урологии) приглашает на прием к урологу. Врач тщательно вас обследует, направит на анализы, ответит на все вопросы. Звоните!
Аденома простаты у мужчин
Аденомой простаты называют широко распространённое урологическое заболевание, также известное под названием доброкачественной гиперплазии предстательной железы (ДГПЖ). Данная патология выявляется у каждого второго мужчины в возрасте 40-50 лет. В отличие от простатита, сопровождающегося воспалительными процессами, при аденоме разрастаются ткани, то есть развивается опухоль. Заболевание приводит нарушению мочеиспускания, семяизвержения и стула, что вносит существенный дискомфорт в повседневную жизнь больного.
Норма ПСА при аденоме простаты
Нормальная концентрация ПСА (Простатического специфического антигена) в крови зависит от возрастной категории. Если для здорового 40-49-летнего человека норма ПСА составляет 2,5 нг/мл, то у мужчин после 70 лет этот показатель увеличивается до 6,5 нг/мл, что тоже считается нормальным. Максимально допустимое содержание ПСА – 10 нг/мл. Более высокий уровень может свидетельствовать об онкологическом заболевании.
Концентрация ПСА у людей, страдающих ДГПЖ, как правило, выше нормы, но она не должна превышать определённого значения, после которого есть вероятность появления раковых клеток. При диагностировании аденомы максимальное повышение концентрации ПСА может достигать 0,75 нг/мл. Более стремительное увеличение этого показателя должно насторожить врача.
Разновидности аденомы
В зависимости от особенностей развития новообразования, гиперплазия предстательной железы может быть:
Ретротригональной – располагается под треугольником мочевика;
Подпузырной – растёт в направлении прямой кишки;
Внутрипузырной – увеличивается в сторону мочевика;
Многоочаговой – сочетает особенности описанных выше видов ДГПЖ.
Кроме того, заболевание подразделяется по стадиям:
I – стадия компенсации, при которой наблюдается увеличение простаты, но при этом не беспокоят болезненные ощущения, и мочевик опорожняется полностью. Протекание болезни на этой стадии может продолжаться от одного года до нескольких лет;
II – стадия субкомпенсации, характеризующаяся неконтролируемым выделением мочи в случае переполненного мочевика и появлением болезненных ощущений;
III – стадия декомпенсации, во время которой протекание заболевания сопровождается болевым синдромом, непроизвольным испусканием мочи. Также могут быть задержки мочеиспускания, ухудшение самочувствия в целом.
Причины появления ДГПЖ
До сих пор учёные не пришли к единому мнению о том, что может провоцировать развитие аденомы простаты. Но всё же есть ряд факторов, способствующих появлению гиперплазии. Среди них:
Возрастные изменения, на фоне которых нарушается гормональный баланс при выработке эстрогенов и андрогенов:
Сидячая работа – по статистическим данным, из 100% мужчин, страдающих ДГПЖ, больше половины приверженцы сидячего образа жизни;
Частые стрессы, конфликты и прочие нагрузки психоэмоционального характера;
Вредные привычки: курение и чрезмерное потребление спиртных напитков;
Симптомы ДГПЖ
О развитии заболевания свидетельствует появление следующих отклонений:
Проблемы с мочеиспусканием;
Сокращение промежутков между позывами, особенно во время сна;
Появление жжения при мочеиспускании;
Непроизвольное подтекание мочи;
Прерывистая струя при мочеиспускании;
Болезненные ощущения при семяизвержении;
Наличие крови и слизи в моче.
Диагностика аденомы
Многие из признаков, характерные для ДГПЖ, могут появляться и при иных урологических заболеваниях. Следовательно, только врач может диагностировать патологию и выбрать способ лечения. Для выявления аденомы простаты применяют разные способы:
Ректальное пальпирование простаты, позволяющее определить патологические изменения: примерное увеличение размеров новообразования, прощупать посредством пальцев аденоматозные узлы и т.д.;
Биохимия крови – направлена на определение концентрации креатинина, по которой можно выявить состояние почек;
Исследование крови на предмет содержания простат-специфического антигена –назначается при подозрениях на онкологию простаты. Также исследования помогают установить вероятность возникновения острой задержки мочи и понять, необходимо ли хирургическое вмешательство;
Общий анализ мочи – позволяет получить представление о наличии/отсутствии других урологических заболеваний;
УЗИ почек и мочевого пузыря – проводится для диагностирования патологических отклонений;
Трансректальное ультразвуковое исследование простаты – основная цель процедуры заключается в выявлении диффузных изменений железы;
Урофлоуметрия – предназначена для определения нарушений процесса испускания мочи;
Уретро-цистоскопические исследования – позволяют исключить прочие патологические отклонения.
Возможные осложнения
Несмотря на то, что аденома является доброкачественным новообразованием, заболевание вовсе не безобидно. Несвоевременное обращение к врачу чревато такими последствиями, как:
Образование камней в мочевике;
Непроходимость мочеиспускательных каналов, на фоне чего может развиться гидронефроз;
Инфекции простаты и мочеиспускательной системы;
Гематурия, сопровождающаяся наличием крови в моче;
Интоксикационный синдром, в результате чего ухудшается общее состояние здоровья;
Острая задержка мочи.
Лечение аденомы
Медикаментозное лечение
Если гиперплазия предстательной железы будет выявлена на ранних стадиях, то для лечения болезни достаточно медикаментозных препаратов. В этом случае назначаются:
Альфа-1-адреноблокаторы – обладают антиспазмирующим действием;
Ингибиторы 5-альфа-редуктазы – предотвращают образование дигидротестостерона, способствующего возникновению и развитию аденоматозного новообразования.
Хирургическое лечение
Хирургическое вмешательство может проводиться с применением разных способов, среди которых:
Открытая аденомэктомия – к данной операции чаще всего прибегают при больших размерах новообразования. По сравнению с другими хирургическими способами, в этом случае существует больший процент вероятности развития осложнений;
Трансуретральная резекция – методика, которая предполагает затрагивание только поражённого участка. То есть удаляется лишь увеличенная часть простаты.
Оперативное лечение
Появление малоинвазивных способов сделало лечение аденомы менее травматичным, но, к сожалению, не во всех случаях их можно применять. К таким способам относятся:
Ударно-волновая терапия – метод, предполагающий применение низкочастотных звуковых волн;
Аппаратная методика – использование аппарата «Андро-гин», позволяющего проводить лечение с помощью электро- и нейростимуляции, цвето-, магнито- и лазеротерапии;
Лазерная хирургия – современный способ, в основе которого лежит использование лазерного луча;
При аденоме ограничено применение некоторых физиотерапевтических процедур, например, основанных на вибрационном воздействии. Сеансы массажа также противопоказаны при ДГПЖ. Массаж предстательной железы эффективен лишь в случае простатита.
Последствия оперативного вмешательства
Любая операция может привести к тем или иным осложнениям, и удаление аденомы не является исключением. Операция может быть осложнена такими симптомами:
Проблемы с мочеиспусканием;
Наличие крови в моче;
Эмболизация аденомы простаты
Эмболизация – безболезненный и эффективный способ удаления ДГПЖ, относящийся к малоинвазивным хирургическим методикам. Во время процедуры выполняется блокировка артериальных сосудов, снабжающих ткани новообразования кровью. После оперативного вмешательства наблюдается уменьшение аденомы и восстановление мочеиспускательных функций.
Неэффективные методы лечения
Аденому предстательной железы бесполезно лечить народной медициной. Ни одно из народных средств (травяных отваров, овощных соков и т.д.) не в состоянии остановить развитие опухоли. Напротив, больной, надеясь на целебную силу потребляемых продуктов, только напрасно потеряет время, которое можно использовать более результативно. Массажные процедуры также неэффективны при ДГПЖ.
Профилактика и прогноз
В качестве профилактических мер, предупреждающих образование аденомы, являются:
Физическая активность, способствующая снижению вероятности застоя крови в организме, в том числе и в органах малого таза;
Отсутствие в мужском гардеробе вещей, которые препятствуют нормальной циркуляции крови в области малого таза (сильно обтягивающих брюк, плавок);
Избавление от лишнего веса – активизирует обменные процессы;
Регулярное посещение врача и контроль уровня ПСА – обязательное мероприятие для мужчин после 40 лет;