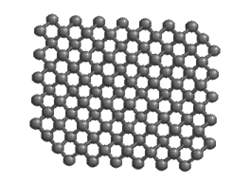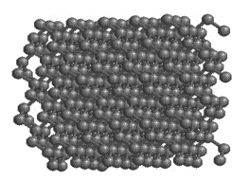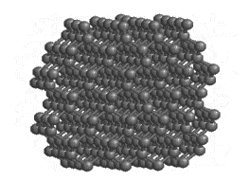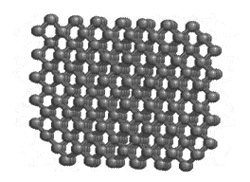
Природа алмаза, графита и угля
Углерод был известен древним народам еще в доисторические времена в виде древесного угля, сажи и каменного угля. По свидетельству римского историка Витрувия, сажа в его время производилась в большом количестве и шла на изготовление краски, применяемой во фресковой живописи, и чернил. Способ получения сажи, по Витрувию, состоял в следующем: смолу, деготь, смолистые щепки, виноградную лозу и подобные материалы сжигали на очаге, а пламя и дым пропускали через отверстия в камеру с мраморными стенками; осевшую сажу снимали и затем растирали с клеем, камедью и купоросом.
С незапамятных времен китайцы пользовались сажей для приготовления туши, которая распространилась затем в Корее, Японии и у народов ближнего Востока (IV в. до н.э.). В Европе тушь стала известна только в XV–XVI вв.
Получение угля также было известно с древнейших времен. Можно считать твердо установленным фактом, что уголь входил в состав употреблявшихся в древности зажигательных веществ.
Самый большой из всех известных алмазов, «Куллинан», найден в 1905 г. в Южной Африке. Его масса 621 г, а размер 10х6х5 см. В Алмазном фонде нашей страны хранится один из самых больших и красивых алмазов в мире – «Орлов» (37,92 г).
Алмазы давно привлекали к себе внимание и из-за других качеств. Еще в древней Индии алмаз служил для обработки драгоценных камней. С той же целью применяли его греки и римляне.
Алхимики не могли пройти мимо этого наивысшего по своей твердости минерала, нерастворимого в кислотах, несгораемого на обычном огне: они и в алмазе искали разгадки «философского камня».
В 1781 г. А.Л.Лавуазье доказал, что при горении угля получается «углекислота» (углекислый газ), которая представляет не что иное, как соединение «химического начала угля» (т.е. элемента углерода) с кислородом.
Истинная природа алмаза была выяснена только в 70-х гг. XVIII столетия, т.е. на пороге великой химической революции. До этого времени никому и в голову не могло прийти, что блестящий минерал, играющий всеми цветами радуги, имеет что-то общее с аморфным и черным углем.
В кратком изложении история установления истинной химической природы алмаза такова.
В XVII в. Аксель де Бут, а затем И.Ньютон высказали предположение, основываясь на сходстве показателей лучепреломления скипидара, камфоры и алмаза, что последний должен гореть.
В 1694 г. флорентийские академики провели опыт сжигания алмаза в фокусе вогнутого зеркала. Они убедились, что алмаз в этих условиях сначала тлеет, как уголь, а потом полностью сгорает. Ф.Лоренц установил затем, что алмаз сгорает без остатка в пламени кузнечного горна.
Все эти опыты вызывали, однако, крайнее недоверие, т.к. общее мнение ювелиров и минералогов сводилось к тому, что алмаз является разновидностью кварца. С выводами о том, что алмаз может гореть, были не согласны и многие крупные химики того времени. Так, например, Г.Руэль (учитель Лавуазье) и некоторые другие химики, проводившие опыты с алмазами, пришли к заключению, что при действии высокой температуры они испаряются.
В 1772 г. Лавуазье совместно с другими учеными провел серию экспериментов по изучению отношения различных тел к нагреванию в фокусе солнечных лучей, собираемых с помощью огромной линзы (около 1,5 м в диаметре).
По результатам исследований он опубликовал два труда «О разрушении алмаза огнем», в которых окончательно доказал, что при сжигании алмаза, как и при сжигании древесного угля, кроме «связывающего воздуха» (углекислого газа), ничего иного не получается и что при горении алмаза также поглощается часть воздуха, как это наблюдалось при горении фосфора или угля.
В 1797 г. английский химик С.Теннант после ряда экспериментов пришел к убеждению, что алмаз – чистейший углерод. Он сжег одинаковые количества алмаза и угля и убедился, что при этом образуются совершенно одинаковые объемы оксида углерода. Этим было доказано, что алмаз – некое видоизменение углерода.
Несколько ранее в 1779 г. шведский химик К.Шееле высказал предположение, что и графит является минеральным углем. Ему удалось позднее, в 1789 г., доказать, что графит хорошо горит в струе водорода, а в 1792 г. он пришел к окончательному выводу, что графит и уголь являются видоизменениями одного и того же элемента.
В 1799 г. Гитон де Морво наблюдал переход алмаза в графит при нагревании первого в сосудах без доступа воздуха. Одновременно он обнаружил, что графит и некоторые другие тела, например кокс, при сгорании дают лишь углекислый газ.
Повторив опыт Теннанта, но дополнив список сжигаемых веществ графитом, де Морво установил важный факт: если подвергать сжиганию равные по весу количества графита, алмаза и угля, то получаются одинаковые количества углекислого газа.
Й.Я.Берцелиус в 1841 г. впервые описал уголь (сажу), алмаз и графит как видоизменения одного и того же элемента и ввел в химию новое понятие «аллотропия».
Латинское название «carboneum» углерод получил от слова «carbo» – уголь, берущего в свою очередь начало от санскритского cra – гореть. Название «графит» (от греч. grapho – пишу) было дано минералогом А.Г.Вернером в 1789 г. после опытов Шееле. В русской литературе графит в начале XVIII в. назывался «карандаш» (от монгольского «кара» – черный, «таш» – камень), а углерод – «углетвором».
Слово «алмаз» и западноевропейское «diamant» – арабского происхождения и означает твердейший. Греки и римляне называли этот минерал adamas. В более или менее измененном виде это слово перешло во все европейские языки. В переводе оно означает неизменный, неукротимый, недоступный, поскольку алмаз не поддавался руке шлифовальщика. Только в XIII в. голландец Ван Беркем догадался шлифовать эти камни друг о друга и таким образом переоткрыл способ шлифовки алмазов, который давно уже был известен в Индии.
Очень любопытна проблема получения искусственного алмаза. Интерес к ней вызывается не только промышленным и экономическим значением этого материала, но и заманчивостью разрешения чисто научной задачи.
Попытки получения алмазов искусственным путем начались сразу после того, как было выяснено, что он является чистейшим углеродом. Они были очень многочисленны. Не будем подробно останавливаться на их описании и назовем лишь некоторые из них.
В 1880 г. английский химик Дж.Хенней получил несколько кристаллов при продолжительном нагревании в железной заваренной трубе легких углеводородов с металлическим литием. Эти кристаллы по своим свойствам могли бы быть отнесены к типу алмаза, в природе, однако, не встречающегося. Эти алмазы и до сих пор хранятся в Британском музее. Проведенное в 1943 г. их рентгенографическое исследование подтвердило, что это действительные алмазы.
Наибольшую популярность получили опыты французского ученого А.Муассана, проведенные им в 1893–1896 гг. Муассан плавил при температуре 2000–3500 °C и высоком давлении железо, к которому он добавлял чистый угольный порошок. Расплавленное железо затем выливалось в полый медный сосуд, охлаждаемый снаружи водой. Застывшая масса обрабатывалась кислотами с целью удаления железа, силикатов, карбида и графита. После этой сложной обработки сплава оставались черные прозрачные кристаллики, царапавшие рубин и сгоравшие в кислороде. Самые крупные из них были в диаметре не более 5 мм. Муассан принял их за алмазы.
Его опыты были повторены многими учеными и всегда приводили к малоубедительным или противоречивым результатам.
По поводу всех попыток получения искусственного алмаза немецкий химик Отто Руфф сделал вывод: «Кроме Муассана никому не удавалось получить искусственный алмаз. Возможно, что Муассан получил его, но это не доказано…».
Однако путь к разрешению проблемы не был закрыт. Дело в том, что большинство опытов производили в то время, когда еще не был решен вопрос о сравнительной устойчивости в земных условиях обеих модификаций углерода – алмаза и графита.
Сотрудник Института химической физики АН СССР О.И.Лейпунский в статье «Об искусственных алмазах» (1939 г.) объяснил, что главная причина неудач исследователей заключалась в том, что «…все попытки изготовления алмаза были сделаны в условиях, при которых графит является более устойчивой твердой фазой, чем алмаз». Ученый рассчитал, что для успешного получения алмаза «во-первых, надо нагреть графит не менее чем до 2000 К», чтобы атомы углерода могли переходить с места на место. Во-вторых, его надо при этом сжать чудовищным давлением, не меньше чем 60 тыс. атмосфер. Тогда он обязательно перейдет в алмаз, подобно тому, как камень, подброшенный рукой, обязательно поднимется в воздух».
Эти теоретические расчеты блестяще подтвердились в 1955 г., когда американским ученым Ф.П.Бэнди, Г.Т.Холлу, Г.М.Стронгу и Р.Г.Венторфу после восьмилетних экспериментов удалось осуществить синтез настоящих алмазов в условиях, близких к названным выше. И все же за один опыт исследователи получали не больше 20 мг алмазов, а самый большой из них имел длину всего 1,2 мм.
В отличие от алмаза искусственный графит получается и используется в промышленности в больших масштабах. Его получают при нагревании угля до температуры 2200–2500 °С в электрической печи. Стоимость производства искусственного графита не превышает стоимости получения естественного графита высокой степени чистоты.
В чем же причина образования из атомов одного и того же элемента столь различных по своим физическим свойствам веществ – твердейшего, блестящего алмаза и мягкого, легко истирающегося черного графита?
Наука дает ныне на этот вопрос точный ответ. В настоящее время твердо установлено, что резкое различие в свойствах алмаза и графита объясняется различием их внутреннего строения.
В кристаллах алмаза все атомы углерода расположены на одинаковых расстояниях друг от друга (1,54 
 |
 |