Системный подход к лечению ХПН и ОПН у кошек и собак
Известно расхожее выражение, что все мы состоим из воды. В сфере диализа жидкостная среда организма так и называется – вода. И у людей, и у животных в ней происходят все биохимические процессы, обеспечивающие полноценную жизнь. Здесь же накапливаются токсины, в том числе уремические, сигнализирующие о патологическом состоянии почек, почечной недостаточности.
Активная вода организма составляет 70 % массы тела. Если же рассматривать ее состав в процентных соотношениях, то в самых больших объемах представлены вода плотных тканей и внутриклеточная вода – 40 и 33 процента соответственно. Далее следует интерстициальная жидкость и лимфа – 12 %. Всего 4,5 процента приходится на долю плазмы крови, по столько же – на воду хрящей и необменную воду костей. Наконец, оставшиеся 1,5 % – трансцеллюлярная вода.
Представим живой организм в виде некой емкости. У нас получится сосуд, разделенный множеством мембран, через которые постепенно просачивается вода. Если она загрязнена, то с течением времени станет грязной жидкость во всем сосуде. Из этого наглядного примера обмена веществ понятно, что при почечной недостаточности мочевые токсины накапливаются не только и не столько в крови, но и во всей активной воде организма – и вся она требует очищения. Об этом следует помнить при расчете дозы гемодиализа. Также не стоит забывать о прямой зависимости времени выравнивания уремических токсинов крови и остальной жидкости от степени дегидратации организма: при обычных условиях процесс занимает порядка четырех часов, в обезвоженной же клетке обмен происходит значительно медленнее.
Снова рассмотрим на примере. Возьмем животное массой 20 кг с мочевиной крови 50 ммоль/литр. Из вышесказанного ясно, что такой же уровень уремической интоксикации будет иметь вся вода организма, а это порядка 14 л жидкости – и необходимо очистить весь этот объем. Очевидно, что плазмаферез, удаляющий 30 процентов плазмы, то есть всего 1,5 % от общей воды, окажется неэффективным, и должно быть принято решение о проведении гемодиализа.
Лечение любого заболевания внутренних органов должно начинаться с создания оптимальных условий, при которых они смогут полноценно выполнять свою работу. Такого же подхода требует и почечная недостаточность у кошек или собак, и, соответственно, нефропротекция. Если почки поражены незначительно, интоксикация начнет снижаться сразу после устранения патологии. Необходимо учитывать и основные факторы, без изменения которых положительные результаты окажутся под вопросом. Остановимся на них более подробно.
Послесловие
За годы работы мы выяснили, что большинство врачей в других клиниках неверно оценивают гемодиализ, считая его крайней мерой. Владельцы, «взращенные» на этом заблуждении, приходят к нам с формулировкой «все остальное не помогло» – и почти все обращения за лечением почечной недостаточности у собак и кошек случаются с опозданием, будь то острая или хроническая формы заболевания.
Уважаемые коллеги и владельцы животных! Бесполезно очищать почки, когда они уже мертвы. Гемодиализ – не волшебное средство, спасающее пациента в последнюю секунду. Назначенный своевременно, он дает врачу необходимые часы и дни для осуществления полноценной нефропротекции.
Допустим, у пациента полностью нарушена фильтрационная способность почек, например, с тотальным ОКН при пироплазмозе. Необходимо восстановить канальцевый эпителий – процесс, зачастую длящийся 15-20 дней. Несмотря на все наши капельницы, собака или кошка может элементарно не дожить до выздоровления, умерев от банальной уремии через неделю. Между тем, к нам часто попадают животные с мочевиной 90-100 и креатинином больше 2 500. Как правило, при таком уровне интоксикации в организме нарастают необратимые процессы системной дегенерации обмена веществ – и изменить что-то бывает уже невозможно.
Существует простой способ оценки эффективности терапии при почечной недостаточности у кошек и собак. В начале лечения у животного берется анализ крови на мочевину с креатинином. Повторите исследование не через 5-7 дней, как это обычно бывает, а через сутки, тогда вы точно будете знать, правильно ли выполнены назначения, все ли патологические факторы учтены. Если показатели растут, почка либо мертва, либо вы что-то упустили. Важно проводить исследования в одной лаборатории, чтобы исключить разницу погрешности измерений, которая скроет истинную суточную динамику.
Не залечивайте животное! Когда терапия назначена правильно, улучшение состояния пациента произойдет уже через 12 часов. Если этого не случилось, значит, упущен какой-то фактор, например, неверно определены степени обезвоживания или истощения, Ph плазмы крови, не учтены анемия, наличие сопутствующей инфекции, хронические заболевания и прочее. В этом случае тактику лечения нужно срочно менять.
Хроническая почечная недостаточность у собак и кошек – не диагноз. Это обязан знать каждый врач – и с этим знанием он должен подходить к каждому нефробольному. ХПН – это синдром, обусловленный гибелью нефронов в почке, который наблюдается от нескольких месяцев до нескольких лет. Причинами этого симптомокомплекса могут быть повышенное артериальное давление, хронический пиелонефрит, гидронефроз, нефросклероз, целый ряд аутоиммунных болезней, сахарный диабет и т.д. Иными словами, любые патологические факторы, приводящие к гибели нефронов, – истинная причина, следствием которой уже является ХПН. И ваша главная задача – находить и устранять их.
Запишитесь на прием или нужна консультация?
Будем рады Вам помочь!
Лечение судорожных припадков: принципы диагностики и терапии
Введение
Судорожные припадки обусловлены пароксизмальными синхронными разрядами нейронов, обычно возникающими в коре головного мозга.
Причины припадков
Идентификация припадков
Диагностика эпилепсии
Наиболее эффективное лечение судорожных припадков возможно только в том случае, когда поставлен диагноз.
Причины возникновения судорожных припадков перечислены в таблице 1. Первичные проявления, анамнез и клинические симптомы позволяют приоритизировать дифференциальные диагнозы и выбрать соответствующие диагностические тесты.4
Если подозревается симптоматическая или реактивная эпилепсия (например, 12-летний золотистый ретривер с припадками, появившимися впервые), рекомендуется полное диагностические обследование, включающее минимальный набор данных, тест на толерантность к желчным кислотам, визуализационные исследования головного мозга и анализ цереброспинальной жидкости. Во многих случаях полное обследование не является необходимым при первом появлении припадков (например, в остальном здоровая 3-летняя немецкая овчарка с недавно появившимися припадками), однако всегда рекомендуются получение минимального набора данных, проведение теста на толерантность к желчным кислотам и офтальмоскопия. Тест на толерантность к желчным кислотам не только исключает портосистемный шунт, но и является исходной мерой функции печени, которую можно использовать впоследствии, если животному будут назначены гепатотоксические препараты, например фенобарбитал.
Всем владельцам животных можно выдать список симптомов, за которыми нужно следить и которые могут свидетельствовать о причинном заболевании головного мозга (изменения в поведении, спотыкание, нарушения зрения) и поэтому требуют более развернутого диагностического обследования.
Судорожные припадки являются наиболее частым и, как правило, единственным симптомом, свидетельствующим о наличии опухоли головного мозга.
Поэтому исключительно важно рекомендовать визуализацию мозга посредством компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) любой собаке старше 6 лет с судорожными припадками, появившимися впервые. Некоторые породы предрасположены к специфическим болезням, следовательно, первичные симптомы также будут определять рекомендации. Например, впервые появившиеся судорожные припадки у 4-летнего боксера с большей вероятностью обусловлены опухолью головного мозга, чем первичной эпилепсией. Сходным образом первое появление припадков у 2-летнего мопса, вероятнее всего, является результатом энцефалита. Кошки более чувствительны к гипертензии и ее последствиям, чем собаки, но у обоих видов животных важно попытаться измерить кровяное давление и исследовать сетчатку на наличие признаков сосудистого или иного заболевания.
Когда лечить судорожные припадки
Большинство судорожных состояний вызывают рецидивирующие припадки, которые по природе являются прогрессирующими из-за постепенного включения дополнительных нейронов в судорожные очаги (киндлинг-эффект). Если первопричина припадков может быть идентифицирована, то лечение должно быть направлено на эту причину. Применение противоэпилептических средств показано, если поставлен диагноз первичной эпилепсии или если лечение первопричины припадков при вторичной эпилепсии не обеспечивает контроль припадков (например, у животных с опухолями головного мозга, гидроцефалией или энцефалитом). До начала лечения важно определить частоту припадков, поскольку противоэпилептические средства имеют побочные эффекты и не всегда являются необходимыми. Например, если лечение припадков начато после первого припадка, то уже никогда не будет ясно, был ли этот припадок единственным, и трудно определить, можно ли прекратить лечение или нет. Исключением из этого правила являются случаи, когда диагноз поставлен и дальнейшие припадки могут угрожать жизни животного. Например, если у животного был один припадок и диагностирована опухоль головного мозга, то последующие припадки могут вызвать фатальное повышение внутричерепного давления, и пациенту следует немедленно назначить противоэпилептические средства.
Общее эмпирическое правило состоит в том, что припадки следует лечить, если они возникают чаще, чем раз в месяц, если они возникают кластерами или сочетаются с эпилептическим статусом, или если они сопровождаются неприемлемыми побочными эффектами (например, исключительно длительным послесудорожным периодом, злобой или обструкцией дыхательных путей у брахицефальных пород собак).
Во всех случаях наиболее эффективное лечение животного требует полного понимания и согласия его хозяина, поэтому до начала лечения важно определить ожидания владельца.
Какой лекарственный препарат использовать у собак
Для лечения судорожных припадков у собак исторически использовали два лекарственных препарата – фенобарбитал и бромид калия. Оба лекарства эффективны как по отдельности, так и в комбинации. Примидон не рекомендован из-за его гепатотоксичности, а диазепам не является эффективным оральным противоэпилептическим средством из-за его короткого периода полувыведения у собак. Период полувыведения фенобарбитала составляет от 48 до 72 часов, и его следует давать перорально два раза в день. Стартовая доза равна 2–4 мг/кг перорально два раза в день, и постоянный уровень препарата в крови достигается за 10–14 дней. Если необходимо быстрое прекращение припадков (например, у собаки болезнь начинается с кластерных припадков), введение дозы, равной 12 мг/кг и распределенной на 24–48 часов, обеспечит терапевтические уровни фенобарбитала в крови, хотя эта доза вызовет временную седацию.
Преимуществами фенобарбитала являются хорошая эффективность, доступность, разумная цена, удобный режим дозирования и быстрота, с которой изменения дозы отражаются в концентрациях в крови, что обеспечивает легкость регулирования дозы.
Недостатками являются необходимость ведения документации (это контролируемый лекарственный препарат), полифагия, полиурия/полидипсия, первоначальная седация (должна пройти примерно через неделю) и седация при необходимости более высоких концентраций препарата в крови, гепатотоксичность (чаще всего связанная с концентрациями в крови, превышающими 35 мкг/мл), нейтропения и тромбоцитопения (очень редкое осложнение), некролитический дерматит и взаимодействие с другими лекарственными препаратами (не следует использовать совместно с циметидином, хлорамфениколом или кетоконазолом). Может развиться толерантность к фенобарбиталу, которая с течением времени потребует более высоких доз для поддержания того же уровня в крови. Терапевтические концентрации в крови лежат в диапазоне 15–45 мкг/мл, хотя концентрации, превышающие 35 мкг/мл, связаны с повышенным риском гепатотоксичности. После достижения стабильного состояния изменения дозы, необходимые для достижения желаемого уровня в крови, можно рассчитать с использованием следующего уравнения: новая доза = текущая доза × желаемый уровень в крови / измеренный уровень в крови. Необходимая доза определяется частотой припадков, концентрацией препарата в крови и тяжестью имеющихся побочных эффектов. Состояние собак, получающих лечение фенобарбиталом, следует контролировать через каждые 6–12 месяцев посредством физикального обследования, измерения концентраций фенобарбитала в крови и биохимического профиля с целью выявления признаков гепатотоксичности. При внезапном резком возрастании концентраций ферментов печени (ожидаемым является их умеренное возрастание при лечении фенобарбиталом) или снижении концентрации альбумина необходимо провести дополнительное исследование в форме теста на толерантность к желчным кислотам.
Следует отметить, что резкое прекращение лечения припадков (фенобарбиталом или бромидом калия) может привести к фатальному эпилептическому статусу или рецидиву припадков, которые гораздо труднее контролировать.
Бромид калия с большим успехом использовали как дополнение к терапии фенобарбиталом у собак с устойчивыми к лечению припадками. В настоящее время его все чаще используют как единственное средство при лечении собак. Бромид калия имеет длительный период полувыведения, колеблющийся в диапазоне от 24 до 46 дней, в зависимости от содержания соли в пищевом рационе и функции почек. Его следует давать один раз в день в дозе, равной 25–40 мг/кг/день, и постоянный уровень в крови достигается через 3–4 месяца. Для более быстрого достижения терапевтических концентраций в крови (100–300 мг/дл) можно нагружать животное этим препаратом в дозе, равной 100–130 мг/кг/день, в течение 5 дней, после чего снизить дозу до поддерживающей, равной 30 мг/кг. Концентрацию в крови следует проверить после 5-дневного применения нагрузочной дозы и через 4–6 недель, чтобы убедиться в том, что терапевтические уровни сохраняются. В экстренных случаях терапевтические уровни могут быть достигнуты за один день посредством орального введения 200 мг/кг с небольшим количеством корма с 2–3-часовыми интервалами (общая доза равна 600 мг/кг).
Преимуществами бромида калия являются хорошая эффективность, особенно при использовании дополнительно к терапии фенобарбиталом, отсутствие гепатотоксичности, дозирование один раз в день, разумная цена и отсутствие статуса контролируемого лекарственного средства.
Недостатками являются полиурия/полидипсия и полифагия, седация и слабость задних конечностей при высоких концентрациях в крови (в частности, в сочетании с фенобарбиталом), отсутствие разрешения на использование в ветеринарии, необходимость постоянного пищевого рациона (изменения содержания соли в пищевом рационе изменяют концентрации препарата в крови), раздражение желудочно-кишечного тракта, состояние кожи, называемое бромодермой, и возможная связь с гиперлипемией и панкреатитом. Бромид калия имеется в продаже в жидкой форме и в форме капсул. Считается, что капсулы с большей частотой вызывают побочные эффекты со стороны желудочно-кишечного тракта, поскольку растворение капсулы обеспечивает фокусирование солевого раствора внутри желудка. Раздражение желудочно-кишечного тракта можно минимизировать посредством дачи лекарства с кормом.
Принимая решение о начале лечения фенобарбиталом, бромидом калия или комбинацией обоих препаратов, следует учесть несколько факторов. Например, если собака очень молодая, то желательно начать лечение бромидом калия, а фенобарбитал добавить только в случае необходимости, чтобы минимизировать время, в течение которого собака получает гепатотоксический препарат. Если заболевание впервые проявилось в форме кластера тяжелых припадков, обычно предпочтительно сразу же начать лечение животного фенобарбиталом, поскольку в этом случае можно быстрее достичь постоянных концентраций в крови, а препарат можно вводить внутривенно. Если владелец животного не может давать препарат через каждые 12 часов, то препаратом выбора может быть бромид калия, поскольку его можно давать через каждые 24 часа. Наконец, следует учитывать побочные эффекты препаратов, и собак с заболеванием печени не следует лечить фенобарбиталом, тогда как использования бромида калия лучше избежать при лечении собак с панкреатитом в анамнезе.
В последнее время в США и Европе более доступными стали препараты Леветирацетам (Кеппра) и Зонисамид (Зонегран), которые можно добавлять к бромиду калия и фенобарбиталу или использовать вместо них.
Зонисамид (Зонегран) – это производное сульфонамида, которое впервые было использовано в Японии в 1989 г. Он лицензирован в Соединенных Штатах Америки с 2000 г., однако дженерики появились только в последнюю пару лет. Механизм действия еще не полностью выяснен, однако, по-видимому, он абсолютно иной, нежели у фенобарбитала и бромида калия. Известно, что он блокирует возбуждающие натриевые и кальциевые каналы, предполагалось, что он является ингибитором карбоангидразы (хотя это не считается важным механизмом регулирования судорожных припадков) и влияет на синтез и распад нейромедиаторов. Он метаболизируется печенью (не через цитохром Р450) и имеет достаточно длительный период полувыведения, равный 18–28 часам, так что его можно давать собакам два раза в день – большое преимущество перед многими другими лекарствами, которые нужно давать чаще.
В исследованиях собак, проведенных в Японии, были определены дозы, необходимые для достижения концентраций в крови, признанных терапевтическими, и было показано, что подходящей стартовой дозой для животных, не получающих фенобарбитал, является доза, равная 5 мг/кг два раза в день, тогда как животным, получающим фенобарбитал, необходима доза, равная 10 мг/кг два раза в день. Дозу можно повышать достаточно безопасно; в исследованиях хронической токсичности для собак дозы до 75 мг/кг/день использовали в течение года с минимальными эффектами на аппетит и массу тела.
Побочные эффекты, отмеченные у собак, которых одновременно лечили дополнительными противоэпилептическими средствами, включали атаксию (реагировавшую на снижение дозы), летаргию и рвоту. Недавно у нас был случай, в котором, по-видимому, развилась идиосинкразическая гепатотоксичность, которая разрешилась после прекращения приема препарата. Опубликованы два исследования клинической эффективности зонисамида как дополнительного средства при лечении стойкой эпилепсии у собак, и в обоих случаях были получены впечатляющие реакции со снижением припадков у 58 % и 82 % собак. Однако эти исследования не были контролируемыми и включали относительно малое количество пациентов. Благодаря безопасности, доступности и практичности дозирования (два раза в день) этот лекарственный препарат в настоящее время является препаратом первого выбора для лечения собак с первичной эпилепсией. Хотя в настоящее время еще нет данных относительно его эффективности при использовании в качестве единственного средства, эти данные, по-видимому, появятся в течение следующих нескольких лет. Базовые концентрации в крови взяты из опубликованных данных, полученных у людей, и определены как 10–40 мкг/мл; концентрации в крови могут быть измерены в лаборатории фармакологии Колледжа ветеринарной медицины Обернского университета, но это довольно дорогостоящая процедура. Однако относительная безопасность данного лекарственного препарата делает мониторинг его концентраций в крови менее критичным, чем при использовании таких препаратов, как фенобарбитал. Мы обычно измеряем концентрацию в крови в том случае, если судорожные припадки плохо контролируются, а доза является высокой: это полезно для того, чтобы определить, поможет ли дальнейшее повышение дозы.
Фармакокинетика и токсичность зонисамида также была исследована на кошках, и, хотя препарат показал себя как безопасный, все же в этом случае нельзя повышать дозы так же, как у собак: примерно у половины кошек, получавших 20 мг/кг/день, развивались летаргия и атаксия, а также симптомы со стороны желудочно-кишечного тракта, такие как анорексия, рвота и диарея. Период полувыведения равен 33 часам, и рекомендована доза, равная 5–10 мг/кг один раз в день.4
Леветирацетам (Кеппра) приобрел популярность вследствие разрешения его использования для лечения людей, выданного в 1999 г. в связи с его безопасностью. Считается, что этот препарат оказывает эффект за счет связывания с синаптическим белком SV2A и ингибирования выделения возбуждающего нейромедиатора. Леветирацетам преимущественно экскретируется почками, а в печени осуществляется минимальный метаболизм, что делает его идеальным выбором для животных с нарушенной функцией печени. Период полувыведения короткий и составляет всего 3,5–6 часов, а дозы по 20 мг/кг три раза в день позволяют достигнуть предложенного стандартного диапазона концентраций в плазме, равного 5–45 мкг/мл, хотя собакам, также получающим фенобарбитал, могут потребоваться более высокие дозы. Опубликовано одно исследование эффективности данного препарата у собак со стойкой эпилепсией, в котором 8 из 14 собак показали снижение частоты припадков более чем на 50 %. Единственным описанным побочным эффектом была седация у одной из собак. (Я обнаружила, что у некоторых пациентов возникает седация при добавлении леветирацетама к другим противоэпилептическим препаратам.) Как и в исследованиях зонисамида, данное исследование не было контролируемым и включало лишь небольшое число собак. Дополнительным преимуществом леветирацетама является то, что он выпускается в форме для внутривенного введения, и поэтому его начинают использовать для лечения пациентов с эпилептическим статусом или кластерными припадками.
Концентрации леветирацетама в плазме могут быть измерены в фармакологической лаборатории в Оберне за ту же цену, что и в случае зонисамида, однако отсутствие побочных эффектов делает эти измерения менее критичными. Кроме того, у людей не было отмечено четкой взаимосвязи между концентрацией в плазме и терапевтическим эффектом. Несмотря на то что препарат обычно применяют в виде дополнительной терапии в устойчивых к лечению случаях, основными препятствиями к его использованию являются неудобство дозирования (три раза в день), а также, как и в случае зонисамида, отсутствие в настоящее время данных о его эффективности в качестве единственного средства.
Леветирацетам использовали для лечения кошек.7 Период его полувыведения равен 3 часам, рекомендованная доза была равна 20 мг/кг три раза в день.
Семь из 10 кошек с устойчивой к лечению эпилепсией ответили на лечение леветирацетамом, и лишь у двух возникли побочные эффекты в виде летаргии и снижения аппетита.
Эпилептическая болезнь
Эпилепсия (эпилептическая болезнь) является хроническим заболеванием головного мозга различной этиологии, которое характеризуется повторными непровоцируемыми приступами нарушений двигательных, чувствительных, вегетативных, психических функций, возникающих вследствие чрезмерных патологических нейронных разрядов. Несмотря на то что существует много причин эпилепсии, в основе заболевания лежат патологические синхронные разряды группы нейронов. Эпилепсия возникает вторично при патологии нейрональных мембран и дисбалансе между возбуждающими тормозящими системами.
Эпиприступ является стрессом для владельца больного животного (CUNNINGHAM, J. C., FARNBACH, G. C. 1988; JAGGY, A., BERNARDINI, M. 1998). Поскольку эпилепсия также распространена у людей, а патогенез и причина некоторых форм эпилепсии все еще остаются неизвестными, собака может послужить моделью исследования патогенеза болезни (STRAUB, H., SPECKMANN, E. J. 1992).
Схематическое объяснение распространения приступа
Тип приступа определяется зоной возбуждения (моторный, сенсорный) с потерей или без потери сознания. «Феномен воспламенения» играет важную роль в терапевтическом обосновании контроля эпилепсии: каждый эпилептический приступ облегчает возникновение следующего, поскольку это вызывает привыкание нейронов к хроническому рецидивирующему возбуждению (эпилептизация мозга) (ENGEL, J., CAHAN, L. 1993).
Конец приступа происходит не из-за нейронного истощения или кислородного дефицита, а в результате активного торможения (HEINEMANN, U., JONES, R.S.G. 1990).
Морфологические изменения, вызванные приступами, установлены в головном мозге у людей и собак. Это глыбчатая нейронная дегенерация в коре головного мозга, гиппокампе и миндалинах (MELDRUM, B.S. 1991).
Парциальные приступы, которые иногда очень трудно распознаваемы, часто наблюдаются у кошек (PODELL, M. 1998; CIZINAUSKAS, S., JAGGY, A. 2004). Приступ появляется внезапно и длится от нескольких секунд до нескольких минут, восстановление может длиться от 24 часов после эпилептического статуса до недели, иногда дольше. Животные дезориентированы и иногда возбуждены, не находят себе места, пытаются идти в любом направлении, возможна центральная слепота.
Частота приступов может сильно варьировать. У некоторых животных приступы регулярны и повторяются циклически, у других могут быть очень нерегулярные интервалы. Интенсивность и продолжительность приступов также очень индивидуальна. Иногда они повторяются сериями. У собак крупных пород приступы обычно протекают тяжелее и частота приступов, как правило, имеет тенденцию к учащению, хотя время, необходимое для констатации факта учащения приступов у некоторых пациентов может составить два-три года или даже больше. Поэтому далеко не всегда необходим контроль приступов после первого проявления заболевания.
Тип течения заболевания может быть разным и в большинстве случаев он характерен для породы (KATHMANN, I., JAGGY, A. 2003; STEFFEN, F., JAGGY, A. 1995; JAGGY, A., HEYNOLD, Y. 1996). Но полностью идентичного течения заболевания не бывает никогда.
Тип наследования: идиопатическая эпилепсия встречается у всех пород и помесей. Примерно у половины всех собак, страдающих от эпилептических приступов, они вызваны идиопатической эпилепсией (JAGGY, A., BERNARDINI, M. 2004).
Однако есть породы, которые подвержены этому заболеванию больше, чем другие: бордер-колли, кокер-спаниель, длинношерстный колли, такса, большая швейцарская горная собака, ирландский сеттер, миниатюрный шнауцер, пудель и жесткошерстный фокстерьер (OLIVER, J. E., LORENZ, M. D., KORNEGAY, J. N. 1997; DE LAHUNTA, A. 1983).
Способ наследования сложен: у большинства пород необходимо изменение более одного гена для наследования эпилепсии (мультифакторное наследование). Пол также играет роль у некоторых пород. Значительное предрасположение было найдено у кобелей следующих пород: гончая, золотистый ретривер, бернский зенненхунд (SRENK, P., JAGGY, A., GAILLARD, C., BUSATO, A., HORIN, P. 1994; KATHMANN, I., JAGGY, A., BUSATO, A., BДRTSCHI, M., GAILLARD, C. 1999; BIELFELT, S. W., REDMAN, H. C., MCCLELLAN, R. O. 1971).
В эпидемиологическом исследовании собак породы лабрадор было обнаружено, что они имеют тенденцию к появлению приступа в определенных ситуациях, особенно после напряжения (HEYNOLD, Y., FAISSLER, D., STEFFEN, F., JAGGY, A. 1997).
Данный вид эпилепсии, скорее всего, необходимо классифицировать не как идиопатический, а как рефлекторный.
Идиопатическая эпилепсия может также встречаться у кошек, хотя эпилептическими приступами они страдают редко (не более 5-10 % всех кошек). (CIZINAUSKAS, S., JAGGY, A. 2004). Причины приступов у кошек совершенно другие и требуют отдельного рассмотрения.
Факт, что наследование идиопатической эпилепсии вовлекает ряд генов, делает выделение носителей невозможным либо весьма сложным. Многие животные – носители одного из генов – не становятся больными и не считаются таковыми. В связи с этим рекомендуют по крайней мере больных животных не допускать к разведению.
Составляющие эпилептического приступа
Непосредственно клинические судороги называют моторным приступом или иктальным периодом (от ictus – приступ, припадок) (Рис. 1).
Аура – наиболее ранняя стадия приступа, которая служит предупреждением. Аура часто наблюдается у животных. Это очень короткий эпизод потери сознания или моторные расстройства, замеченные непосредственно перед эпилептическим приступом («приступ перед приступом»). В настоящее время полагают, что аура является парциальным приступом.
В одном исследовании пятнадцати собак породы лабрадор с идиопатической эпилепсией благодаря использованию видеокамеры аура была зарегистрирована у каждой собаки (HEYNOLD, Y., FAISSLER, D., STEFFEN, F., JAGGY, A. 1997).
Период, наступающий сразу после судорог, называется постиктальным периодом (Рис. 2), интервал между судорогами – интериктальным периодом (Рис. 3). Все эти периоды имеют отображение на ЭЭГ.
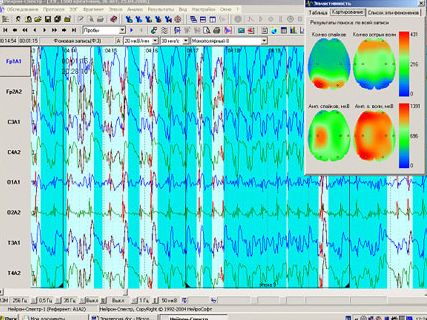
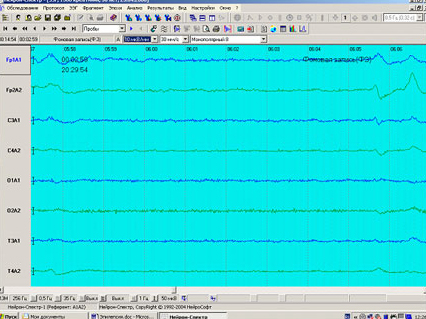
Рис. 2. Постиктальный период. Собака беспородная, 13 лет
Постиктальный период характеризуется замешательством, дезориентацией, слюноотделением, блужданием, неугомонностью, нечувствительностью и некоторой слепотой. Одни собаки быстро приходят в сознание, но какое-то время могут быть угнетены, спят. Другие же, находясь в состоянии спутанного сознания, возбуждены, вскакивают, натыкаются на предметы, скулят. Длительность этой стадии зависит от тяжести иктального периода и может продолжаться в течение нескольких дней, после чего состояние постепенно нормализуется.
Очень важно, что вне приступов может не быть постоянного очага эпилептической активности, он появляется только непосредственно перед приступом. Напротив, наличие очага эпилептической активности не означает, что собака страдает этим заболеванием.
Эпилепсия представляет собой большую группу нозологически самостоятельных форм, имеющих строго определенные клинические проявления, лечение и прогноз.
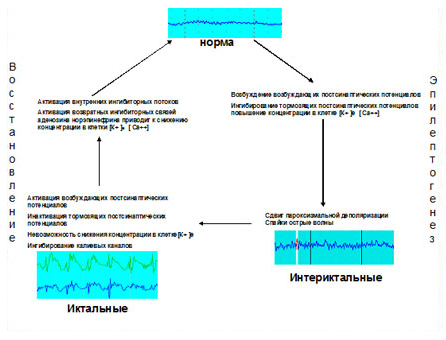
Основными механизмами эпилептогенеза
являются уменьшение ГАМК-эргического ингибирования и усиление глутаматэргического возбуждения. Дисбаланс между процессами торможения и возбуждения в головном мозге приводит к развитию вторичных изменений нейронов, их метаболизму. Изменения характеризуются разрастанием аксонов и повреждением дендритов, индукцией факторов роста нервной ткани и гормонов-модуляторов, модификацией ионных и клеточных рецепторов, каналов.
Под симптоматическими формами понимаются эпилептические синдромы с известной этиологией и верифицированными морфологическими нарушениями (опухоли, рубцы, дисгенезии и др.). При идиопатической эпилепсии отсутствуют симптомы органического поражения ЦНС, структурные изменения в головном мозге по данным нейровизуализации и сведения о больных эпилепсией среди кровных родственников пациента. При этом идиопатическая форма рассматривается как самостоятельное, генетически детерминированное заболевание.
Имеющиеся механизмы, приводящие к переходу интериктальной стадии в иктальную, показаны на Рис. 4.
Класcификация форм эпилепсии
Классификация форм эпилепсии на сегодняшний день в ветеринарной медицине не разработана. Для классификации можно использовать различные принципы: локализацию эпилептического очага, характер клинических проявлений, глубину расстройств сознания, электроэнцефалографические характеристики и др.
Разделение форм эпилепсии по основному виду приступов: генерализованные или фокальные. Генерализованные формы эпилепсии характеризуются судорогами вследствие первичной активации нейронов обоих полушарий мозга. Фокальные (очаговые) эпилепсии протекают с приступами, возникающими при раздражении группы нейронов в одном полушарии. Данный вид классификации невозможен без ЭЭГ.
Далее эпилепсии делят по этиологии: идиопатические, симптоматические и наследственные (выявляются из анамнеза и сведений о родителях и щенках с родственными связями).
Идиопатическими эпилепсиями называют заболевания, возникающие спонтанно по неясной или неизвестной причине.
Под симптоматическими подразумевались эпилептические синдромы с известным этиологическим фактором. Симптоматическая эпилепсия является одним из симптомов другого заболевания нервной системы: дизгенезии, последствие гипоксически-ишемического поражения мозга и др. и определяется после применения методов нейровизуализации ( МРТ, КТ).
Наследственные эпилепсии изучены недостаточно, можно предположить наследственный путь передачи заболевания по анамнезу наличия в линии разведения подобных случаев заболевания. Наследуются полигенно с различной степенью экспрессивности. Рефлекторная эпилепсия, передающаяся как генетическое заболевание, описана чешскими авторами (Martinek, Horak, 1970).
Встречаются и имеют широкое распространение у домашних животных эпилептиформные приступы, не связанные с эпилепсией, а вызванные травмой, опухолью, гидроцефалией, гипогликемией либо воспалительным процессом различной этиологии в центральной нервной системе (вирусы, микроорганизмы, паразитарные заболевания), различными интоксикациями (отравление нейротоксинами и некоторыми лекарственными средствами, такими как декарис (левамизол), хлорорганические и фосфорорганические соединения, гексахлорофен, этиленгликоль, карбамат, стрихнин и ртуть). Кризы, вызываемые данными токсинами, часто носят генерализованный и билатеральный характер с начала их действия (то есть не относятся к парциальным кризам) (А. В. Хохлов, 2007).
Причиной эпилептиформных приступов могут быть нарушения работы внутренних органов, например уремия, гепатоэнцефалопатия, нарушения электролитного баланса, недостаток кальция у молодых животных. Вышеперечисленные заболевания имеют свой патогенез, и у них нет ничего общего с эпилепсией, кроме проявлений: тонические или тонико-клонические судороги, расстройства поведения.
Большой клинической ошибкой будет постановка диагноза только по наличию эпилептиформных приступов, так как в ряде случаев такой подход только оттягивает время, лишая пациента возможности излечения.
Классификация эпилепсий у собак, используемая автором
Генуинная эпилепсия (идиопатическая) заболевание, при котором явное органическое поражение головного мозга отсутствует. Данная форма эпилепсии обусловлена нарушением функции собственно головного мозга. К этой группе относимы случаи с отсутствием признаков органического повреждения мозга.
Идиопатическая генерализованная эпилепсия. Для всех форм идиопатической эпилепсии характерны:
Криптогенная генерализованная эпилепсия
Криптогенной эпилепсией называют синдромы с неуточненной, неясной этиологией. Подразумевается, что криптогенные формы являются симптоматическими, однако на современном этапе при применении методов нейровизуализации не удается выявить структурные нарушения в головном мозге.Проявляется у собак в возрасте старше 5 лет.
Симптоматическая эпилепсия. Симптоматическая эпилепсия является одним из симптомов другого заболевания нервной системы: дизгенезии, последствия гипоксически-ишемического поражения мозга и др.
Кора на разрезе или на МРТ может казаться тонкой, нерегулярной или, наоборот, более толстой, чем нормальной. Диагноз может только быть подтвержден гистологической экспертизой.
 Эпилептические синдромы
Эпилептические синдромы
К группе эпилептических синдромов можно отнести заболевания, возникшие после травмы.
Травматическая эпилепсия
Последствия черепно-мозговой травмы, любого повреждения мозга даже при том, что первичное поражение мозга уже давно клинически вылечено, но ткань мозга заместилась рубцовой тканью, и с течением времени сформировался очаг эпилептической активности.
Встречается у всех пород собак и кошек.
Классификация эпилептических приступов:
Общие принципы диагностики
Критериями диагностики эпилепсии являются повторные спонтанные приступы и характерные изменения при ЭЭГ-исследовании. Без ЭЭГ невозможно провести диагностику эпилепсии. Минимальными требованиями для диагностики являются: объективное описание приступов, детализация клинической структуры, продолжительность, частота и другие характеристики приступа, анамнестические сведения и первичное обследование. В основу диагностики положено соотношение клинических и электроэнцефалографических данных. Дополнительные сведения о наследственной отягощенности, данные прижизненной визуализации головного мозга необходимы для выяснения этиологии эпилептического синдрома. Обязательны сведения о наличии любой наследственной отягощенности, информация о предшествующем лечении. Выявляются этиологические особенности заболевания, сопутствующие неврологические и психические расстройства, а также побочные эффекты проводимой противосудорожной терапии.
Диагностические процедуры
Электроэнцефалографическое исследование
Рутинное электроэнцефалографическое исследование проводится при всех видах приступов и подразумевает одновременную регистрацию не менее 8 каналов ЭЭГ. Дополнительные каналы используются для наблюдения за сердечным ритмом, дыханием, мышечной активностью, движением глаз и т.д. Базовая ЭЭГ-запись проводится на протяжении не менее 20 минут. Пробы с гипервентиляцией, фотостимуляцией и исследования во время сна требуют более продолжительной регистрации ЭЭГ, особенно гипервентиляция крайне редко может быть проведена у собак и практически никогда у кошек. Провокационные процедуры (звукостимуляция, фотостимуляция) позволяют оценить влияние на ЭЭГ некоторых раздражителей. Фотостимуляция является обязательным требованием при проведении ЭЭГ-исследования. Хотя точной интерпретации полученных данных на сегодняшний день нет.
Пароксизмальные ЭЭГ-паттерны могут быть зафиксированы в момент проведения пробы и по ее окончании. На рис Рис. 6 и 7 хорошо заметны изменения на энцефалограмме после введения пропофола.
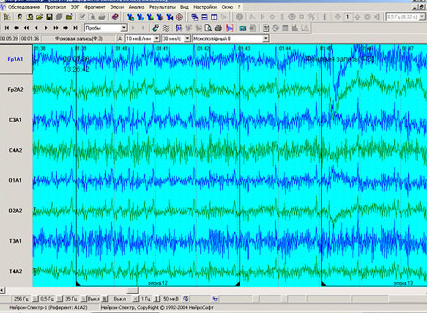
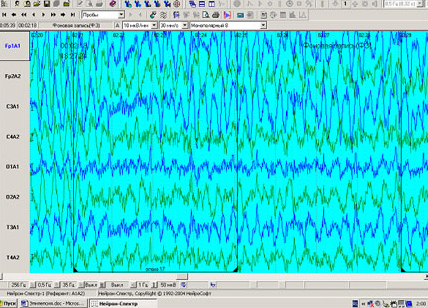
Рис. 7. Та же собака породы померанский шпиц с гидроцефалией с введенным пропофолом. Собака находится в наркозе
ЭЭГ-мониторинг
ЭЭГ-мониторинг заключается в долговременной регистрации активности головного мозга и проводится с помощью игольчатых электродов. ЭЭГ-сигналы записываются и сохраняются на компьютере. Долговременная запись ЭЭГ рассматривается как необходимое исследование в специализированной клинике.
Показания к ЭЭГ-мониторингу:
Методы нейровизуализации
Нейрорадиологические методы, в отличие от ЭЭГ-исследований, не могут ни подтвердить, ни опровергнуть диагноз эпилепсии. Они неинформативны для цели собственно диагностики эпилепсии, но предназначены для установления этиологии заболевания и для ведения предоперационного периода.
Показания для обязательного проведения компьютерной томографии (КТ) или магнитно-резонансной томографии:
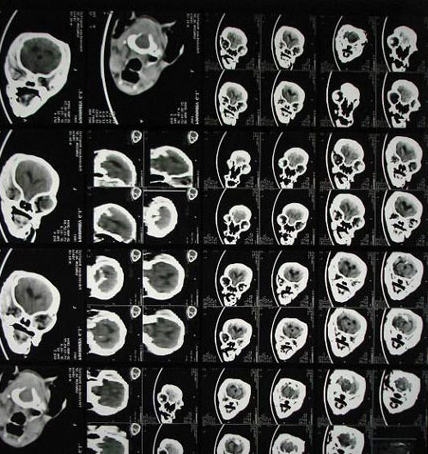
КТ собаки породы йоркширский терьер, данный метод малоинформативен в сравнении с МРТ у той же собаки)
МР-томография информативна в отношении гиппокампального склероза, кортикальных дисплазий, микродисгенезий, гетеротопий, а также небольших поверхностных повреждений ткани мозга.
Лабораторные методы исследования
Диагностика этиологии эпилептических синдромов и период подбора антиконвульсантов (объем обследований):
Другие диагностические методы
К ним относятся: 24-часовой ЭКГ-мониторинг, анализ цереброспинальной жидкости; биопсия кожи, мышц, печени, костного мозга и головного мозга.
Но важно помнить, что даже при условии определения портосистемного шунта наличие эпилептических приступов может быть совсем не по причине гепатоэнцефалопатии.
Принципы медикаментозной терапии
Основная цель фармакотерапии эпилепсии – предотвратить развитие приступов без возникновения острых или хронических побочных эффектов противоэпилептических препаратов. Выбор лекарственного средства определяется характером приступа и типом течения эпилептического синдрома. Лечение следует всегда начинать с одного антиэпилептического препарата первой очереди выбора, показанного для данной формы эпилепсии. Доза медикамента повышается еженедельно до достижения терапевтического эффекта, высшей дозы или возникновения побочных эффектов. Для купирования эпилептического статуса рекомендуются следующие парентеральные препараты: диазепам, фенобарбитал, пропофол. При этом купирование должно осуществляться преимущественно одним препаратом. Многие противосудорожные препараты имеют взаимный антагонизм и одновременное их применение может значительно ослабить противосудорожный эффект каждого.
Есть в основном три группы антиконвульсантов, разделенных согласно их механизму ослабления активности приступа:
Основные мишени ПЭП:
Если нет результата от лечения фенобарбиталом, возможно использование других препаратов (primidone, felbamate, gabapentin, levetiracetam, zonisamide, pregabalin, carbamazepine или clorazepate), хотя эти препараты не настолько эффективны и не изучены их дозирование, возможные побочные эффекты (KATHMANN, I., JAGGY, A. 2003; PODELL, M. 1998).
В настоящее время для людей синтезировано около 30 противосудорожных препаратов, обладающих различным спектром антиконвульсантной активности.
Однако действие этих препаратов на собак неизвестно.
В России практические врачи мало знакомы с антиэпилептическими препаратами и принципами лечения эпилепсии. Требуется специализация, так в гуманной медицине не менее 50 пациентов должно находиться у врача на контроле одновременно.
Для качественного лечения нужна специализация и в ветеринарии. В большинстве случаев имеет место назначение препаратов, не обладающих антиэпилептической активностью, а также массы дополнительных сопутствующих средств, взаимодействие которых не изучено.
Лечение эпилепсии должно быть индивидуальным: лечат не болезнь, а больного.
Как не бывает двух идентичных осколков у одинаковых стаканов, упавших с одной высоты, так не бывает идентичных больных эпилепсией.
Купирование эпилептических приступов должно осуществляться преимущественно одним препаратом.
С появлением хроматографических методов определения уровня антиконвульсантов в крови стало очевидным, что многие противосудорожные препараты имеют взаимный антагонизм и одновременное их применение может значительно ослабить противосудорожный эффект каждого. Кроме того, монотерапия позволяет избежать возникновения тяжелых побочных проявлений, частота которых значительно возрастает при назначении нескольких препаратов одновременно. Использование политерапии (2-х препаратов) возможно лишь в случае абсолютной неэффективности монотерапии. Применение двух антиэпилептических препаратов может быть приемлемо лишь в единичных случаях при резистентных формах эпилепсии и должно быть строго аргументировано.
Одновременное применение более трех антиконвульсантов при лечении эпилепсии категорически недопустимо!
Первые противоэпилептические препараты были обнаружены случайно. К ним относятся фенобарбитал (ФБ), фенитоин (ФТ), примидон (ПМД), бензодиазепины, этосуксимид, сультиам и вальпроат; позже их назвали ПЭП 1-го поколения. С 1990 г. в клинику стали внедряться ПЭП 2-го поколения: фелбамат, вигабатрин (ВГБ), ЛТД, ГБП, ТПМ, тиагабин (ТГБ), ОКС, леветирацетам (ЛТЦ), ПГБ и ЗНС. Эффекты фенобарбитала, как и других барбитуратов, обусловлены способностью усиливать и/или имитировать тормозящее действие GABA на синаптическую передачу. В России, в связи с недоступностью чистого фенобарбитала, приходится применять препараты его содержащие; не лучшее решение, но другого практически нет.
Корвалол
1 таблетка содержит действующие вещества:
Международное название: Этиловый эфир альфа-бромизовалериановой кислоты.
Паглюферал
Содержит кофеин, что тоже не слишком хорошо.
1 таблетка содержит действующие вещества:
Для контроля эпилептических приступов могут быть использованы другие препараты:
Внимание! НАТРИЯ ХЛОРИД строго противопоказан при использовании бромидов.
Лечение эпилепсии должно осуществляться в зависимости от формы эпилепсии, а не от характера приступов
При отсутствии эффекта от терапевтической дозы в течение 1 месяца необходимо дальнейшее постепенное увеличение дозы препарата до получения выраженного положительного эффекта или появления нежелательных явлений.
Таким образом, лечение эпилепсии может быть достаточно эффективным при соблюдении целого ряда условий:
Согласно полученных нами данных, наиболее частыми причинами недостаточного терапевтического эффекта являются:
Принципы отмены антиконвульсантов
При тяжелых формах эпилепсии (симптоматическая парциальная эпилепсия) данный период увеличивается до 3-4 лет.
Не существует единого мнения по вопросу о тактике отмены антиконвульсантов. На наш взгляд, отмена препаратов опасна.В нашей практике часты случаи рецидива с гораздо худшими последствиями! Лечение может быть отменено постепенно в течение 12 месяцев или одномоментно, по усмотрению врача.
Те же принципы лечения могут быть применены к кошкам, но стоит отметить, что фенитоин (период полураспада у кошек – 24-108 часов в отличие от 3-4 часов у собак) и primidone ядовиты для кошек, диазепам может использоваться у кошек, но лишь в начале терапии, пока не установится эффективная концентрация фенобарбитала в крови.
Важно помнить, что период полураспада этих препаратов у кошек значительно длиннее, чем у собак, и нет привыкания, характерного для собак.
Противопоказания
Принципы хирургического лечения эпилепсии
Любое нейрохирургическое вмешательство, главной целью которого является уменьшение частоты эпилептических приступов, может быть расценено как хирургическое. Хирургическое лечение показано при фармакорезистентной эпилепсии. Предоперационная оценка включает клиническое и энцефалографическое подтверждение фокальной зоны эпилептогенеза с определением локализации и анатомического размера по данным МР-томографии.
Причины гибели при эпилепсии
Большинство владельцев считает, что во время приступа собака нанесет себе какие-то серьезные повреждения, на самом деле это крайне редко. Эпилептический статус очень опасен в связи с выраженной мышечной активностью: тонико-клонические судороги дыхательной мускулатуры, аспирация слюны из ротовой полости, задержки и аритмии дыхания ведут к гипоксии и ацидозу; сердечно-сосудистая система испытывает нагрузки в связи с мышечной работой; неадекватный газообмен в легких вызывает гипоксию, гипоксия усиливает отек мозга. Ацидоз приводит к нарушению гемодинамики и микроциркуляции. Вторично все больше ухудшаются условия для работы мозга.
Два основных механизма ведут к цитотоксическому действию и некрозу, в них клеточная деполяризация поддерживается стимуляцией НМДА—глютамат-рецепторов, и ключевым моментом является запуск внутри клетки каскада разрушения:
В первом случае чрезмерное нейрональное возбуждение является результатом отека (жидкость и катионы поступают внутрь клетки), ведущее к осмотическому повреждению и клеточному лизису.
Во втором случае активация НМДА-рецепторов активирует поток кальция в нейрон с аккумуляцией внутриклеточного кальция до уровня выше, чем вмещает цитоплазматический кальцийсвязывающий протеин. Свободный внутриклеточный кальций является токсичным для нейрона и ведёт к серии нейрохимических реакций, включающих митохондриальные дисфункции, активирует протеолиз и липолиз, уничтожающие клетку. Этот механизм и лежит в основе гибели при эпистатусе.
Сайт, предоставляющий информацию и поддержку тем, чьи питомцы (кошки или собаки) страдают эпилепсией. Перейти на сайт >





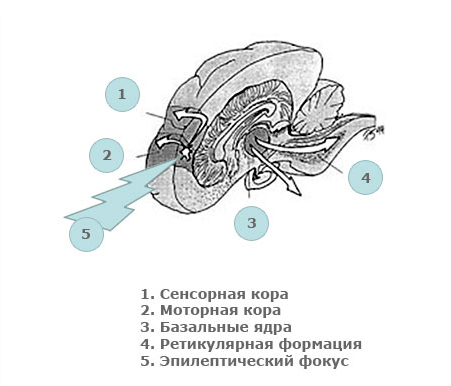
 Эпилептические синдромы
Эпилептические синдромы






